题目内容
6.反应C(s)+H2O?CO(g)+H2(g)△H>0,达到平衡时,下列说法正确的是( )| A. | 增大C的量,H2O的转化率增大 | |
| B. | 减小容器体积,正、逆反应速率均减小 | |
| C. | 加入催化剂,平衡常数不变 | |
| D. | 升高温度,平衡向逆反应方向移动 |
分析 A.碳的状态为固体,改变固体浓度,不影响化学平衡;
B.减小容积,增大了压强,反应速率增大;
C.催化剂不影响化学平衡;
D.该反应为吸热反应,升高温度后平衡向着正向移动.
解答 解:A.由于C的状态为固体,则增大C的量,化学平衡不发生移动,故A错误;
B.减小容器容积,容器内压强增大,则正逆反应速率都增大,故B错误;
C.加入催化剂后,化学平衡不发生移动,则化学平衡常数不变,故C正确;
D.升高温度后,平衡向着吸热的反应方向一定,该反应的正反应为吸热反应,则平衡向着正向移动,故D错误;
故选C.
点评 本题考查了化学平衡的影响因素,题目难度中等,明确浓度、温度、催化剂等因素对化学平衡的影响为解答关键,注意掌握影响化学平衡的因素,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
17.下列反应的离子方程式中,书写正确的是( )
| A. | Fe与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 实验室制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 铜与稀硝酸反应:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
14.等容积的四个密闭容器中进行同样的反应2A(g)+B(g)?3C(g)+2D(g).起始时,A、B的物质的量分别如表所示( )
| 甲 | 乙 | 丙 | 丁 | |
| A | 2 | 1 | 2 | 1 |
| B | 1 | 1 | 2 | 2 |
| A. | A的转化率为:甲<丙<乙<丁 | B. | A的转化率为:甲<乙<丙<丁 | ||
| C. | B的转化率为:甲>丙>乙>丁 | D. | B的转化率为:丁>乙>丙>甲 |
1.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的一种药物,已知其结构简式是
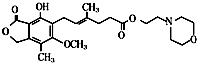
则下列关于MMF的说法中,不正确的是( )
①MMF所有原子一定处在同一平面;
②可以跟溴水加成;
③可以被KMnO4酸性溶液氧化;
④可以跟NaHCO3溶液反应;
⑤MMF的分子式为C24H31O7N;
⑥可以发生消去反应;
⑦可以发生加聚反应;
⑧可以发生水解反应;
⑨可以发生取代反应.

则下列关于MMF的说法中,不正确的是( )
①MMF所有原子一定处在同一平面;
②可以跟溴水加成;
③可以被KMnO4酸性溶液氧化;
④可以跟NaHCO3溶液反应;
⑤MMF的分子式为C24H31O7N;
⑥可以发生消去反应;
⑦可以发生加聚反应;
⑧可以发生水解反应;
⑨可以发生取代反应.
| A. | ①③⑦⑧ | B. | ③④⑥⑦ | C. | ①④⑤⑥ | D. | ②④⑤⑧ |
11.用0.1000mol•L-1NaOH溶液滴定未知浓度的HCl溶液,下列叙述正确的是( )
| A. | 酸式滴定管在装酸液前未用待装液润洗2~3次,使测定结果偏大 | |
| B. | 滴定终点时,俯视读数,使测定结果偏小 | |
| C. | 只能选用酚酞作指示剂 | |
| D. | 滴入最后一滴NaOH溶液,溶液突然变色,即为滴定终点 |
18.羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)?COS(g)+H2(g)K=0.1.反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法不正确的是( )
| A. | 通入CO后,正反应速率逐渐增大 | |
| B. | 升高温度,H2S浓度增加,表明该反应是放热反应 | |
| C. | 反应前H2S物质的量为7mol | |
| D. | CO的平衡转化率为20% |
15.以下化学反应的产物种类与反应物的浓度、用量和反应条件均无关的是( )
| A. | NH3通入AlCl3溶液中 | B. | Cu与硝酸反应 | ||
| C. | CO2通入NaOH溶液中 | D. | Na与O2反应 |
16.有A.B.C.D.E五种短周期主族元素,原子序数依次增大,其中A是宇宙中含量最高的元素,其原子核中无中子,B,D同主族,且B、D最外层电子数之和与A、C的质子数之和相等.C是同周期中原子半径最大的主族元素,下列说法不正确的是( )
| A. | E的单质不具有漂白能力 | |
| B. | A2D与DB2可发生氧化还原反应,氧化产物与还原产物的质量比为2:1 | |
| C. | A2D的还原性弱于AE的还原性 | |
| D. | B与C形成的两种离子化合物中,阴、阳离子个数比相等且所含化学键类型不完全相同 |