题目内容
10.下列溶液中与50mL 1mol•L-1的AlCl3溶液中氯离子浓度相等的是( )| A. | 150 mL 2 mol•L-1的NaCl | B. | 75 mL 2 mol•L-1的NH4Cl | ||
| C. | 150 mL 3 mol•L-1的KCl | D. | 75 mL 2 mol•L-1的CaCl2 |
分析 1mol•L-1的AlCl3溶液中氯离子浓度为1mol/L×3=3mol/L,结合物质构成、溶质浓度计算离子浓度,以此来解答.
解答 解:A.2 mol•L-1的NaCl中氯离子浓度为2mol/L,故A不选;
B.2 mol•L-1的NH4Cl中氯离子浓度为2mol/L,故B不选;
C.3 mol•L-1的KCl中氯离子浓度为3mol/L,故C选;
D.2 mol•L-1的CaCl2中氯离子浓度为2mol/L×2=4mol/L,故D不选;
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握物质的构成、离子浓度与溶质浓度的关系为解答的关键,侧重分析与计算能力的考查,注意离子浓度与溶液体积无关,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
20.下列溶液:①硝酸钡溶液 ②碘水 ③酸性高锰酸钾溶液 ④氯化铁溶液 ⑤品红溶液,其中能用来区别SO2和CO2气体的是( )
| A. | ③⑤ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②③④⑤ |
1.下述根据下列操作现象或事实,所得结论正确的是( )
| 实验操作及现象 | 实验结论 | |
| A | 分别向2mL 0.1mol•L-1 CH3COOH溶液和2mL 0.1mol•L-1 H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 | 酸性:CH3COOH>H2CO3>H3BO3 |
| B | 向2mL 0.1mol•L-1 NaOH溶液中滴加3滴0.1mol•L-1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1mol•L-1 FeCl3溶液,出现红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| C | 过氧化钠用于呼吸面具中作为氧气的来源 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
| D | 向含有淀粉的FeI2溶液中滴加足量的氯水后变蓝 | 还原性:I->Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
18.下列各组离子在给定条件下能大量共存的是( )
| A. | 在pH=1的溶液中:NH4+、K+、CO32-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- | |
| C. | 无色透明水溶液中:K+、Ba2+、I-、NO3- | |
| D. | 与铝粉反应有氢气生成的溶液中:Na+、Cl-、SO42-、HCO3- |
5.化学基本概念及原理在化学反应中应用广泛.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
已知△H2=+41kJ•mol-1,则△H3=-220kJ•mol-1;平衡常数K3=$\frac{{K}_{1}}{{K}_{2}}$(用K1、K2表示).
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.
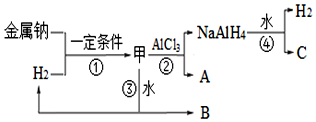
①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 745 | 465 | 413 |
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.

①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.
19.硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等.利用方铅矿精矿( PbS)直接制备硫酸铅粉末的流程如图1:
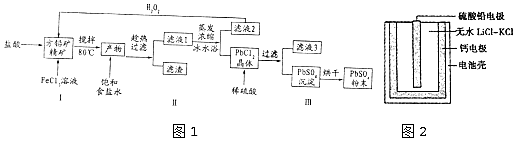
已知:(i) PbCl2 (s)+2C1-(aq)═PbCl42-(aq)△H>0
(ii)有关物质的Ksp和沉淀时的pH如表:
(1)步骤I反应加入盐酸后可以观察到淡黄色沉淀生成,请写出的离子方程式PbS+2Fe3++2Cl-=PbCl2+2Fe2++S↓.
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因用冰水浴使吸热反应PbCl2(s)+2Cl-(aq)?PbCl4-(aq)逆向移动,使PbCl4-不断转化为PbCl2晶体而析出.
(3)在上述生产过程中可以循环利用的物质有FeCl3和盐酸.
(4)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式PbCl2(s)+SO42-(aq)?PbSO4(s)+2Cl-(aq).
(5)PbSO4热激活电池可用作火箭、导弹的工作电源.基本结构如图2所示,其中作为电解质的无水LiCl-KC1混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.
①放电过程中,Li+向正极移动(填“负极”或“正极”).
②负极反应式为Ca+2Cl--2e-═CaCl2.
③电路中每转移0.2mol电子,理论上生成20.7g Pb.

已知:(i) PbCl2 (s)+2C1-(aq)═PbCl42-(aq)△H>0
(ii)有关物质的Ksp和沉淀时的pH如表:
| 物质 | Ksp | 物质 | 开始沉淀时pH | 完全沉淀时pH |
| PbSO4 | 1.0×10-8 | Fe(OH)3 | 2.7 | 3.7 |
| PbCl2 | 1.6×10-5 | Fe(OH)2 | 6 | 7.04 |
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因用冰水浴使吸热反应PbCl2(s)+2Cl-(aq)?PbCl4-(aq)逆向移动,使PbCl4-不断转化为PbCl2晶体而析出.
(3)在上述生产过程中可以循环利用的物质有FeCl3和盐酸.
(4)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式PbCl2(s)+SO42-(aq)?PbSO4(s)+2Cl-(aq).
(5)PbSO4热激活电池可用作火箭、导弹的工作电源.基本结构如图2所示,其中作为电解质的无水LiCl-KC1混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.
①放电过程中,Li+向正极移动(填“负极”或“正极”).
②负极反应式为Ca+2Cl--2e-═CaCl2.
③电路中每转移0.2mol电子,理论上生成20.7g Pb.
3.下列说法正确的是( )
| A. | 常温常压下,22.4L Cl2中含有的分子数为6.02×1023个 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的pH减小 | |
| C. | 氢氧燃料电池工作时,H2在负极上失去电子 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强 |
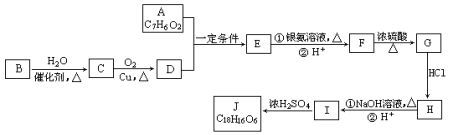
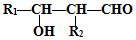
 ,G中含氧官能团的名称羟基、羧基.
,G中含氧官能团的名称羟基、羧基. $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$  +2H2O.
+2H2O.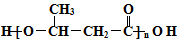 的路线图
的路线图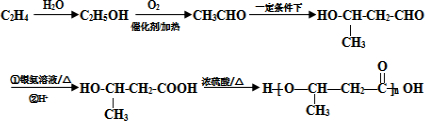 (提示:路线图的书写方法RCH=CH2
(提示:路线图的书写方法RCH=CH2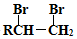 $→_{水/加热}^{NaOH}$
$→_{水/加热}^{NaOH}$ 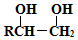 )
)