题目内容
7.下列说法中,正确的是( )| A. | 标准状况下,22.4 L水中含有6.02×1023个水分子 | |
| B. | 32 g氧气所含的原子数目为2×6.02×1023 | |
| C. | 常温常压下,0.5×6.02×1023个一氧化碳分子所占的体积是11.2 L | |
| D. | 1 molCaCl2溶于水配成1 L溶液,所得溶液中Cl-的物质的量浓度为1 mol/L |
分析 A.气体摩尔体积使用对象为气体;
B.由n=$\frac{m}{M}$、N=nNA结合分子构成计算;
C.常温常压下,气体的摩尔体积不知道;
D.Cl-的物质的量浓度是CaCl2浓度的2倍.
解答 解:A.标况下,水是液体,不能使用气体摩尔体积,故A错误;
B.32 g氧气的物质的量为n=$\frac{m}{M}$=$\frac{32g}{32g/mol}$=1mol,则所含的原子数目为2×6.02×1023,故B正确;
C.常温常压下,气体的摩尔体积不知道,无法利用n=$\frac{V}{{V}_{m}}$计算,故C错误;
D.Cl-的物质的量浓度是CaCl2浓度的2倍,则1 molCaCl2溶于水配成1 L溶液,所得溶液中Cl-的物质的量浓度为2 mol/L,故D错误.
故选B.
点评 本题考查了物质的量计算、阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
相关题目
18.某实验小组利用如图装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式.
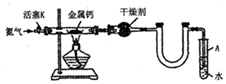
(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
①计算得到实验式CaxN2,其中x=$\frac{14}{5}$.
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.

(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.15 |
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.
2.某同学进行下列实验:下列说法合理的是( )
| 装置 | 操作 | 现象 |
 | 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
| A. | 烧杯A中发生反应:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O | |
| B. | 红棕色气体消失只与NO2和烧杯C中的KI发生反应有关 | |
| C. | 烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关 | |
| D. | 若将铜片换成铁片,则C中的液体也可能变蓝 |
19.已知2SO2(g)+O2(g)?2SO3(g)△H=-198.0 kJ•mol-1.若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是( )
| A. | 该反应条件下,初始时向容器中充入2molSO2和1molO2,反应平衡时,可以释放198.0 kJ的热量 | |
| B. | 达到平衡时,SO2和SO3的浓度一定相等 | |
| C. | 反应体系中,当混合物的密度保持不变,反应达到平衡 | |
| D. | 增大压强和升高温度有利于加快反应速率,但升高温度对平衡转化率不利 |
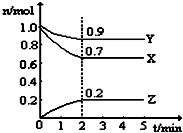 某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: