题目内容
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)=C(金刚石)△H=+1.90kJ?mol-1 可知,金刚石比石墨稳定 |
| C、一定条件下,将0 5 mol N2(g)和1.5 molH2 (g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H═-38.6kJ?mol-1 |
| D、在稀溶液中,H+(aq)+OH-(aq)═H2O(Ⅰ)△H=-57.3kJ?mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ |
考点:反应热和焓变,有关反应热的计算
专题:
分析:A、硫固体变化为蒸气吸热,蒸气发生燃烧;
B、物质能量越高越活泼;
C、反应是可逆反应不能进行完全;
D、浓硫酸溶解过程放热.
B、物质能量越高越活泼;
C、反应是可逆反应不能进行完全;
D、浓硫酸溶解过程放热.
解答:
解:A、等物质的量的硫蒸气和硫固体分别完全燃烧,硫固体变化为蒸气吸热,前者放出热量多,故A错误;
B、由C(石墨)=C(金刚石)△H=+1.90kJ?mol-1 可知,金刚石能量高,石墨比金刚石稳定,故B错误;
C、将0 5 mol N2(g)和1.5 molH2 (g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,反应是可逆反应不能进行彻底,热化学方程式中是全部反应放出热量,故C错误;
D、浓硫酸溶解过程放热,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ,故D正确;
故选D.
B、由C(石墨)=C(金刚石)△H=+1.90kJ?mol-1 可知,金刚石能量高,石墨比金刚石稳定,故B错误;
C、将0 5 mol N2(g)和1.5 molH2 (g)置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,反应是可逆反应不能进行彻底,热化学方程式中是全部反应放出热量,故C错误;
D、浓硫酸溶解过程放热,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ,故D正确;
故选D.
点评:本题考查了化学反应能量变化的分析判断,注意可逆反应的特征分析,物质性质的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
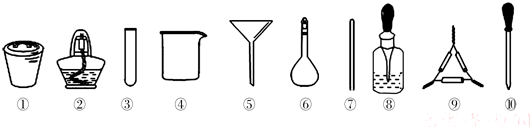
茶叶中铁元素的检验可经过以下四个步骤完成:将茶叶灼烧灰化→用浓硝酸溶解茶叶灰→过滤得到的滤液→检验滤液中的Fe3+.如图是可能用到的实验用品.
有关该实验的说法中正确的是( )

有关该实验的说法中正确的是( )
| A、第一步需选用仪器①、②和⑨,①的名称叫钳埚 |
| B、第二步用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦ |
| C、要完成第三步,需选用④、⑤和⑦,除夹持仪器外还缺滤纸 |
| D、第四步,若滤液中含有Fe3+,加入⑧中的溶液后滤液会显红色 |
下列关于物质用途的说法正确的是( )
①晶体硅是良好的半导体材料,可以制成光电池;
②2CO(g)=2C(s)+O2(g)△H>0该反应可在高温下自发进行;
③氢氟酸可以用来刻蚀玻璃;
④纯净的二氧化硅是制备光导纤维的原料;
⑤利用氯气的毒性可以消灭田鼠;
⑥将Fe(OH)3胶体和泥水分别进行过滤,发现均不能通过滤纸孔隙.
①晶体硅是良好的半导体材料,可以制成光电池;
②2CO(g)=2C(s)+O2(g)△H>0该反应可在高温下自发进行;
③氢氟酸可以用来刻蚀玻璃;
④纯净的二氧化硅是制备光导纤维的原料;
⑤利用氯气的毒性可以消灭田鼠;
⑥将Fe(OH)3胶体和泥水分别进行过滤,发现均不能通过滤纸孔隙.
| A、②④⑤⑥ | B、①③④⑤ |
| C、①②④⑥ | D、③④⑤⑥ |
下列各选项所描述的两个量中,前者一定大于后者的是( )
| A、NH4NO3溶液中NH4+和NO3-的数目 |
| B、纯水在80℃和25℃时的pH |
| C、pH与体积都相同的氨水和NaOH溶液分别用0.1 mol?L-1盐酸恰好中和,所需的盐酸体积 |
| D、相同温度下,pH=12的NaOH溶液和Na2CO3溶液中由水电离出的c (OH-) |
生活处处有化学.下列说法正确的是( )
| A、厨房中用的食盐、食醋都是电解质 |
| B、大量燃烧化石燃料是造成雾霾天气的重要原因 |
| C、盐类都可做调味品 |
| D、浓硫酸可以用来雕刻玻璃制工艺品 |
下列叙述中正确的是( )
| A、将KI和FeCl3溶液棍合,溶液变棕黄色,说明还原性Fe2+>I- |
| B、NO2通入FeSO4溶液中的过程中由浅绿色变为黄色 |
| C、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| D、SO2通入BaCl2溶液中先有白色沉淀后沉淀溶解 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A、X的最高价氧化物对应水化物的酸性比W的弱 |
| B、Y分别与Z、W形成的化合物中化学键类型相同 |
| C、原子半径大小顺序:r(Z)>r(W)>r(X)>r(Y) |
| D、Y的气态简单氢化物的热稳定性比W的弱 |
能正确表示下列反应的离子方程式的是( )
| A、钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
| B、NH4HCO3溶于过量的浓KOH溶液中:NH4++OH-═NH3↑+H2O |
| C、甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应:CH3OH+H2O+6e-═CO2↑+6H+ |
| D、酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |