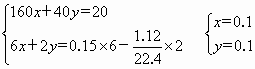题目内容
| |||||||||||||||||||
解析:
(1) |
答案:加少量KClO3,插上Mg条并将其点燃,Fe 精析:铝热反应是指单质Al和某些金属氧化物发生的反应,反应过程中放出大量热,但该反应需要较高的温度才能引发.在混合物上加少量KClO3并插上Mg条,点燃Mg后放出热量,使KClO3分解放出O2,进一步加剧Mg的燃烧,可在短时间内使混合物温度迅速升高,引发反应.发生的反应为Fe2O3+2Al |
(2) |
答案:Fe2O3+6HCl 精析:Fe2O3和MgO都是碱性氧化物,能和酸反应生成盐和水. Fe2O3+6HCl |
(3) |
答案:Fe+2H+ 精析:混合物中只有Fe2O3能和Al发生铝热反应,生成Fe单质.C溶液中有反应产生的FeCl3,还有未反应的HCl.发生的离子反应为:Fe+2H+ |
(4) |
答案:0.67 mol·L-1,2.3 mol·L-1 精析:设试样A中含Fe2O3为x mol,MgO为y mol ∴n(Fe3+)=0.2 mol n(Mg2+)=0.1 mol ∴c(Mg2+)= 根据Fe+2Fe3+ ∴n(Fe2+)=0.05+3×0.1=0.35 c(Fe2+)= |

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案