题目内容
20.下列化学反应可以设计成原电池的是( )| A. | 2H2+O2═2H2O | B. | H++OH-═H2O | ||
| C. | .CaCO3═CaO+CO2↑ | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
分析 据原电池的形成条件中“能自发的发生氧化还原反应”判断.
解答 解:A、2H2+O2═2H2O反应中,反应前后有元素化合价的变化,且该反应是自发进行的氧化还原反应,所以能设计成原电池,故A正确;
B、H++OH-═H2O反应中,反应前后各元素的化合价不变,所以不是发生氧化还原反应,不能设计成原电池,故B错误;
C、CaCO3═CaO+CO2↑反应中,反应前后有元素化合价的变化,但该反应不是自发的进行的氧化还原反应,所以不能设计成原电池,故C错误;
D、Na2CO3+2HCl═2NaCl+H2O+CO2↑反应中,反应前后各元素的化合价不变,所以不是发生氧化还原反应,不能设计成原电池,故D错误;
故选A.
点评 本题是考查原电池的设计,难度不大,明确原电池的构成条件是解本题的关键.

练习册系列答案
相关题目
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1mol 18O含有的中子数为10NA | |
| B. | 22.4L甲烷气体中所含分子数目为NA | |
| C. | 1L 0.1mol•L-1NH4Cl 溶液中NH4+数目为 0.1NA | |
| D. | 1L pH=1的醋酸溶液中,CH3COOH分子的数目为0.1NA |
3.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表所示:
计算该温度下此反应的化学平衡常数为多少?
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
8.对于平衡体系:aA(g)+bB(g)?cC(g)+dD(g)(正反应放热),有下列判断,其中正确的是( )
| A. | 若温度不变,容器体积扩大一倍,A的浓度是原来的0.45倍,则a+b>c+d | |
| B. | 若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为b:a | |
| C. | 若平衡体系中共有气体n mol,再向其中充入bmolB,达到平衡时气体总物质的量为n+bmol,则a+b=c+d | |
| D. | 若a+b=c+d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变 |
15.BaSO4的分子量为233,Ksp=1.0×10-10,把1.0mmol的BaSO4配成10dm3溶液,BaSO4没有溶解的量是( )
| A. | 0.0021g | B. | 0.021g | C. | 0.21g | D. | 2.1g |
5.下列关于Cl2性质的说法正确的是( )
| A. | 密度比空气小 | B. | 是无色无味的气体 | ||
| C. | KOH溶液、活性炭都能吸收氯气 | D. | 能使干燥的有色布条褪色 |
12.下列有机物名称正确的是( )
| A. | 2,2,3-三甲基丁烷 | B. | 2-乙基戊烷 | ||
| C. | 2-甲基-1-丁炔 | D. | 2,2-二甲基-1-丁烯 |
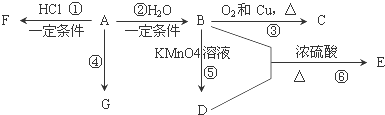
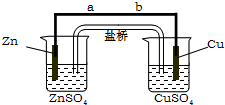 某学生利用下面实验装置探究盐桥式原电池的工作原理.按照实验步骤依次回答下列问题:
某学生利用下面实验装置探究盐桥式原电池的工作原理.按照实验步骤依次回答下列问题: