题目内容
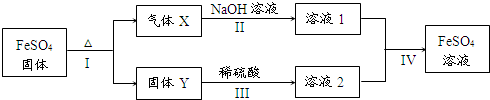
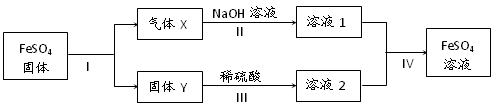
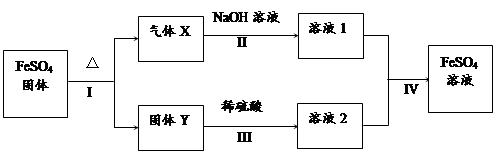
有关FeSO4的转化关系如下图所示(无关物质已略去)。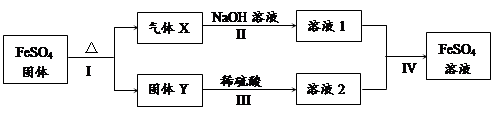
已知:① X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,
产生白色沉淀。
② Y是红棕色的化合物。
(1)气体X的成分是(填化学式) 。
(2)反应I的反应类型属于(填序号) 。
a.分解反应 b.复分解反应 c.置换反应 d.化合反应 e.氧化还原反应
(3)溶液2中金属阳离子的检验方法是 。
(4)若经反应I得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol/L NaOH溶液完全吸收,则反应IV中生成FeSO4的离子方程式是 。
(1)SO2、SO3 (2)a、e
(3)取少量溶液2于试管中,滴加几滴KSCN溶液,溶液变红,则证明原溶液中含有Fe3+。
(4)2Fe3++SO32-+H2O=2Fe2++SO42-+2H+
解析试题分析:X能使品红溶液褪色说明X中含有SO2,但SO2与氯化钡溶液不反应,所以X中还有SO3;Y为红棕色固体说明Y为Fe2O3;反应I为FeSO4受热分解生成SO2、SO3、Fe2O3,既是分解反应又是氧化还原反应;溶液II为Fe2(SO4)3溶液,用KSCN溶液检验Fe3+;反应I得到16gFe2O3,由得失电子相等得生成0.1molSO2,所以生成SO3也为0.1mol。0.1molSO3与0.2molNaOH完全反应,0.1molSO2与0.2molNaOH恰好完全反应生成Na2SO3,溶液I中含有Na2SO3和Na2SO4,反应IV离子方程式为2Fe3++SO32-+H2O=2Fe2++SO42-+2H+。
考点:元素及其化合物性质 氧化还原反应 化学基本反应类型 离子的检验 离子方程式的书写
点评:SO2与NaOH溶液可能生成Na2SO3或NaHSO3。

 优学名师名题系列答案
优学名师名题系列答案