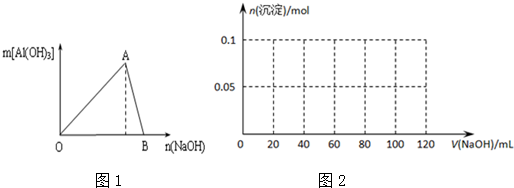
题目内容
6.在明矾溶液中逐滴加入Ba(OH)2溶液,不可能发生的反应的离子方程式是( )| A. | Al3++SO42-+Ba2++3OH-→BaSO4↓+Al(OH)3↓ | |
| B. | Al3++2SO42-+2Ba2++4OH-→BaSO4↓+AlO2- | |
| C. | 2 Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓ | |
| D. | 4Al3++7SO42-+7Ba2++14OH-→7BaSO4↓+2Al(OH)3↓+2AlO2- |
分析 在明矾溶液中逐滴加入Ba(OH)2溶液,当氢氧化钡不足时,反应生成硫酸钡和氢氧化铝沉淀,反应的离子方程式为:①Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓;当氢氧化钡过量时,反应生成偏铝酸钠和硫酸钡沉淀,反应的离子方程式为:②Al3++2SO42-+2Ba2++4OH-→BaSO4↓+AlO2-,当氢氧化钡稍过量时,反应生成硫酸钡、氢氧化铝沉淀和偏铝酸钠,结合反应①②进行分析.
解答 解:A.氢氧化钡不足时,反应生成硫酸钡和氢氧化铝沉淀,但钡离子与氢氧根离子的物质的量之比应该为1:2,正确的反应为:2Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓,故A错误;
B.当氢氧化钡过量时,氢氧化铝溶解生成偏铝酸钠,反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-→BaSO4↓+AlO2-,故B正确;
C.当氢氧化钡不足时,反应生成硫酸钡和氢氧化铝沉淀,反应的离子方程式为:2 Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓,故C正确;
D.当氢氧化钡稍过量,反应生成硫酸钡、氢氧化铝沉淀和偏铝酸钠,可能的反应为:4Al3++7SO42-+7Ba2++14OH-→7BaSO4↓+2Al(OH)3↓+2AlO2-,故D正确;
故选A.
点评 本题考查了离子方程式的书写方法,为高考的高频题,题目难度不大,注意掌握离子方程式的书写原则,根据反应物过量情况正确判断生成物为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
16.下列指定反应的离子方程式正确的是( )
| A. | 铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ | |
| B. | 向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H+═2Fe3++3H2O | |
| D. | 向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42-+20H+═4Fe3++3O2↑+10H2O |
17.铝是金属元素,某同学认为铝也有一定的非金属性.能支持该观点的下列描述是( )
| A. | 氢氧化铝能溶于强碱溶液 | B. | 铝片能与盐酸反应生成氢气 | ||
| C. | 氯化铝溶液显酸性 | D. | 铝能发生铝热反应 |
14.削过皮的苹果过一段时间后颜色就会由白色变为褐色,食品科学上称为“褐变”.某研究性学习小组查阅有关资料,发现不同文献解释不同.
I、《化学教学》:苹果中Fe2+被空气中的O2氧化成Fe3+而变色.
II、《中学化学教学参考》:苹果中的酚类物质在苹果中的氧化酶催化下被空气中的O2氧化而生成有色物质.
已知酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色.如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色.
(1)为探究苹果“褐变”是否为I的原因,该小组同学设计了如下实验:
①刚削皮的苹果立刻滴上2~3滴A溶液,继而再滴上几滴氯水.
②在“褐变”后的苹果上滴上2~3滴A溶液.
回答下列问题:
A溶液是KSCN溶液(填化学式).若I的解释正确,写出①中有关的离子方程式:2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3 此空删去;上述①②的实验现象应为:①滴加A溶液时,无明显现象,再滴加几滴氯水,变红色;②变红色.经实验,①②均无明显现象,说明观点I的解释是错误的.
(2)为探究苹果“褐变”是否为II的原因,该小组同学又设计了如下实验.请帮他们在表中完善实验③、④探究目的和结论.
I、《化学教学》:苹果中Fe2+被空气中的O2氧化成Fe3+而变色.
II、《中学化学教学参考》:苹果中的酚类物质在苹果中的氧化酶催化下被空气中的O2氧化而生成有色物质.
已知酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色.如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色.
(1)为探究苹果“褐变”是否为I的原因,该小组同学设计了如下实验:
①刚削皮的苹果立刻滴上2~3滴A溶液,继而再滴上几滴氯水.
②在“褐变”后的苹果上滴上2~3滴A溶液.
回答下列问题:
A溶液是KSCN溶液(填化学式).若I的解释正确,写出①中有关的离子方程式:2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3 此空删去;上述①②的实验现象应为:①滴加A溶液时,无明显现象,再滴加几滴氯水,变红色;②变红色.经实验,①②均无明显现象,说明观点I的解释是错误的.
(2)为探究苹果“褐变”是否为II的原因,该小组同学又设计了如下实验.请帮他们在表中完善实验③、④探究目的和结论.
| 序号 | 实 验 步 骤 | 现 象 | 探究目的和结论 |
| ③ | 将刚削皮的苹果立刻放入隔绝空气的环境中 | 相当长一段时间内,无明显变化 | 探究目的:探究空气中的O2对苹果“褐变”的影响 结论:“褐变”是苹果中的某些物质与空气中的O2发生反应,生成有色物质.(或没有空气O2的参与,苹果不发生“褐变” |
| ④ | 将刚削皮的苹果立刻放入90℃~95℃的水中2min,再放在空气中. 再将另一块刚削皮的苹果立刻放入稀盐酸中浸泡2min后取出洗净,再放在空气中.将盐酸改为酒精、醋酸铅溶液进行相同实验. | 相当长一段时间内,均无明显变化 | 探究目的:探究氧化酶对苹果“褐变”的影响 结论:经加热或稀盐酸浸泡,酶变性而失去催化能力,没有氧化酶的催化,苹果不发生“褐变”.(或苹果发生“褐变”,必须在氧化酶的催化下才能发生. . |
| ⑤ | 在刚削皮的苹果上滴加FeCl3溶液. | 苹果由白色变为绿色 | 探究目的:探究苹果中是否含有酚类物质. 结论:苹果中含有酚类物质. |
1.分子式为C5H12O的醇,将其充分氧化可生成饱和一元羧酸,这种醇的可能结构有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
6.由黄铜矿(CuFeS2)制取铜的简单流程如图:

下列说法正确的是( )

下列说法正确的是( )
| A. | 由CuFeS2生成Cu2S,SO2和铁的氧化物反应中硫元素被还原 | |
| B. | 熔炼过程中的主要反应为:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2 | |
| C. | 铜的电解精炼过程中纯铜做阳极 | |
| D. | 上述冶炼过程产生大量SO2,通常用饱和NaHSO3溶液吸收 |
3.试验中,下列实验操作正确的是( )
| A. | 用试管取试剂瓶中的碳酸钠溶液时,发现取量过多,为了不浪费立即把多余的试剂倒入原试剂瓶中 | |
| B. | 硝酸钡溶于水,故可将含硝酸钡的废液倒入水槽,再用水冲入下水道 | |
| C. | 用蒸发的方法使氯化钠从溶液中析出,应将蒸发皿中的氯化钠溶液全部加热蒸干 | |
| D. | 稀释浓硫酸时,将浓硫酸缓缓注入水中,并不断搅拌 |