题目内容
(6分)实验室常用的浓盐酸物质的量浓度约为12.0mol·L-1。
(1)实验室欲用上述浓盐酸配制480mL 0.20 mol·L—1 的稀盐酸溶液,则需要取上述浓盐酸 mL。
(2)配制过程中,不需要的仪器(填写代号) 。
A.药匙 B.胶头滴管 C.玻璃棒 D.烧杯
完成实验还缺少的仪器是 、 。
(3)取用任意体积的所配0.20 mol·L-1 HCl溶液时,下列物理量中不随所取体积的多少而变化的是 (填字母)
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl—的数目 D.溶液的密度
(1)8.3(1分) (2)A(1分) 500mL容量瓶(1分) 10mL量筒(1分)(3) BD(2分)
【解析】
试题分析:(1)实验室中没有480mL容量瓶,配制480mL 0.20 mol·L—1 的稀盐酸应用500mL容量瓶,所配溶液的体积应为500mL,根据稀释定律,稀释前后溶质HCl的物质的量不变,令需要浓盐酸的体积为V,则:V×12.0mol?L-1=500mL×0.20mol?L-1,解得V≈8.3mL;(2)配制步骤有量取、溶解、移液、洗涤、定容、摇匀等操作,用10mL量筒量取浓盐酸,在烧杯中稀释,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯与玻璃棒2~3次,并移入容量瓶内,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞,反复颠倒摇匀,所需要的仪器有:玻璃棒、10mL量筒、胶头滴管、烧杯、500mL容量瓶,故不需要的仪器为:A.药匙;还缺少的玻璃仪器是:500mL容量瓶、10mL量筒;(3)取用任意体积的所配0.20 mol·L-1 HCl溶液时,A、根据n=cV判断溶液中HCl的物质的量随溶液体积的变化而变化;B、溶液的浓度不随体积变化而变化;C、溶液中Cl—的数目随溶液体积的变化而变化;D.溶液的密度不随体积变化而变化,选BD。
考点:考查一定物质的量浓度溶液的配制。

 阅读快车系列答案
阅读快车系列答案下列数据是对应物质的熔点
Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
据此做出的下列判断中错误的是
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
 NaAlO2(aq)
NaAlO2(aq) Al(OH)3 ②S
Al(OH)3 ②S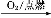 SO3
SO3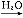 H2SO4
H2SO4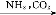 NaHCO3
NaHCO3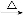 Na2CO3
Na2CO3 FeCl3(aq)
FeCl3(aq) Mg(OH)2
Mg(OH)2 MgO
MgO