题目内容
标况下,6.5g的锌与足量的盐酸反应,生成氢气的物质的量为多少?氢气的体积是多少?
考点:化学方程式的有关计算
专题:计算题
分析:根据n=
计算6.5g Zn的物质的量,根据方程式:Zn+2HCl=ZnCl2+H2↑,计算生成氢气的物质的量,根据V=nVm计算氢气的体积.
| m |
| M |
解答:
解:6.5g Zn的物质的量=
=0.1mol,
设生成氢气的物质的量为x,则:
Zn+2HCl=ZnCl2+H2↑
1 1
0.1mol x
x=
=0.1mol
标况下,生成氢气的体积=0.1mol×22.4L/mol=2.24L,
答:生成氢气的物质的量为0.1mol,氢气的体积是2.24L.
| 6.5g |
| 65g/mol |
设生成氢气的物质的量为x,则:
Zn+2HCl=ZnCl2+H2↑
1 1
0.1mol x
x=
| 0.1mol×1 |
| 1 |
标况下,生成氢气的体积=0.1mol×22.4L/mol=2.24L,
答:生成氢气的物质的量为0.1mol,氢气的体积是2.24L.
点评:本题考查化学方程式的计算,比较基础,有利于基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法中,不正确的是( )
| A、相对分子质量相同,组成元素的百分含量相同的不同有机物一定是同分异构体的关系 |
| B、碳原子数相同、结构不同的烷烃一定是互为同分异构体关系 |
| C、两有机物互为同系物,则它们也是互为同分异构体关系 |
| D、碳原子数≤10的烷烃,其一氯代物没有同分异构体的烷烃有4种 |
下列有关反应类型说法中正确的是( )
A、由乙二醇制取高分子 是通过加聚反应完成的 是通过加聚反应完成的 |
| B、乙醇在浓硫酸作催化剂,并且加热的条件下一定发生消去反应 |
| C、卤代烃一般来说在NaOH的水溶液中能发生取代反应,而在NaOH的醇溶液中不一定能发生消去反应 |
| D、酯类物质在一定条件下水解一定得到相应的羧酸和醇 |
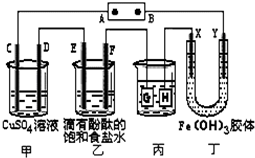 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.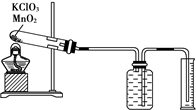 某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.实验步骤如下:
某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.实验步骤如下: