题目内容
19.X、Y、Z、R、W是原子序数依次增大的短周期主族元素,X与Z同主族,X的原子半径最小,Y与R 同主族,Y最外层电子数是电子层数的3倍.下列叙述正确的是( )| A. | 原子半径:W>R>Z | B. | 最高价氧化物对应水化物酸性:R>W | ||
| C. | X与W形成的是离子化合物 | D. | 气态氢化物的热稳定性:Y>R |
分析 X、Y、Z、R、W是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,则X为H元素;Y最外层电子数是电子层数的3倍,则含有2个电子层,最外层电子数为6,为O元素;X与Z同主族,Z的原子序数大于O,则Z为Na;Y与R 同主族,则R为S元素;W原子序数大于S,故W为Cl,结合元素周期律解答.
解答 解:X、Y、Z、R、W是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,则X为H元素;Y最外层电子数是电子层数的3倍,则含有2个电子层,最外层电子数为6,为O元素;X与Z同主族,Z的原子序数大于O,则Z为Na;Y与R 同主族,则R为S元素;W原子序数大于S,故W为Cl.
A.同周期从左向右原子半径在减小,则原子半径为Z(Na)>R(S)>W(Cl),故A错误;
B.非金属性W(Cl)>R(S),故W的最高价氧化物对应的水化物酸性比R的强,故B错误;
C.W与X形成物质为HCl,属于共价化合物,故C错误;
D.非金属性Y(O)<R(S),非金属性越强,氢化物的稳定性越强,Y的气态氢化物的热稳定性比R的强,故D正确,
故选D.
点评 本题考查结构性质位置关系应用,侧重分析推理能力与元素周期律的考查,根据原子结构和元素在周期表中的位置推断元素是解题关键,难度中等.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
9.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
10.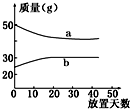 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如右图所示,分析a、b曲线变化的原因是( )| A. | a升华、b冷凝 | B. | a蒸发、b吸水 | C. | a蒸发、b潮解 | D. | a冷凝、b吸水 |
4.下列有关物质应用的叙述中,不正确的是( )
| A. | 氢氧化铝可用于治疗胃酸过多 | |
| B. | ClO2用于饮用水消毒 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | Si用于制造光导纤维 |
11.下列关于化学反应与能量的说法中不正确的是( )
| A. | 反应Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3•H2O+8H2O过程中的能量变化情况符合如图 | |
| B. | 氢氧燃料电池的总反应为:2H2+O2=2H2O | |
| C. | 化学平衡状态指的是反应物和生成物浓度不再改变时的状态 | |
| D. | 催化剂既能加快化学反应速率,又能提高原料利用率或转化率 |
8.分子中碳与氢两元素的质量比为24:5的烃的一氯代物共有( )
| A. | 4种 | B. | 3种 | C. | 6种 | D. | 5种 |
16.在同温同压下,相同体积的氢气和氦气具有相同的( )
| A. | 原子数 | B. | 质量 | C. | 中子数 | D. | 质子数 |