题目内容
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物.
(1)冶炼铜的反应为:8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号).
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
除去Al3+的离子方程式是 .
(3)为验证炉渣中含有FeO,先将炉渣用稀酸溶解,再在酸性条件下加入适当的氧化剂.(提供的试剂:稀盐酸、稀硫酸、KSCN溶液、酸性KMnO4溶液、NaOH溶液、碘水)所选试剂为 、 ,证明炉渣中含有FeO的实验现象为 .
(4)配平上述反应的离子方程式(氧化性物质依据你的选择填入[])
Fe2++ H++ []→ Fe3++ []+ H2O
(5)如果证明炉渣中是否含有FeO,将炉渣溶于稀硝酸,每含有1mol FeO,可产生气体的体积是 L(标准状况,假设硝酸的还原产物只有NO).
(6)Fe2O3可以作为染料,也可进一步制得净水剂Fe2(SO4)3,Fe2(SO4)3的净水原理是 (用相应的方程式表示).
(1)冶炼铜的反应为:8CuFeS2+21O2
| 高温 |
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
除去Al3+的离子方程式是
(3)为验证炉渣中含有FeO,先将炉渣用稀酸溶解,再在酸性条件下加入适当的氧化剂.(提供的试剂:稀盐酸、稀硫酸、KSCN溶液、酸性KMnO4溶液、NaOH溶液、碘水)所选试剂为
(4)配平上述反应的离子方程式(氧化性物质依据你的选择填入[])
(5)如果证明炉渣中是否含有FeO,将炉渣溶于稀硝酸,每含有1mol FeO,可产生气体的体积是
(6)Fe2O3可以作为染料,也可进一步制得净水剂Fe2(SO4)3,Fe2(SO4)3的净水原理是
考点:铜金属及其重要化合物的主要性质,氧化还原反应方程式的配平,含硫物质的性质及综合应用,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:(1)8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2中,Fe元素的化合价升高,Cu、O元素的化合价降低;
(2)过量的氢氧化钠与铝离子反应生成偏铝酸根离子;
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象来解答;
(4)亚铁离子被高锰酸钾氧化为铁离子,然后根据电子得失和电荷守恒配平;
(5)FeO于稀硝酸反应的方程式可知3FeO~NO,然后求解;
(6)Fe2(SO4)3,Fe2(SO4)3的净水原理是得用铁离子的水解,生成氢氧化铁胶体.
| ||
(2)过量的氢氧化钠与铝离子反应生成偏铝酸根离子;
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象来解答;
(4)亚铁离子被高锰酸钾氧化为铁离子,然后根据电子得失和电荷守恒配平;
(5)FeO于稀硝酸反应的方程式可知3FeO~NO,然后求解;
(6)Fe2(SO4)3,Fe2(SO4)3的净水原理是得用铁离子的水解,生成氢氧化铁胶体.
解答:
解:(1)8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2中,Fe元素的化合价升高,Cu、O元素的化合价降低,则Cu、O元素被还原,故答案为:Cu、O;
(2)过量的氢氧化钠与铝离子反应生成偏铝酸根离子,方程式为Al3++4OH-═AlO2-+2H2O,故答案为:Al3++4OH-═AlO2-+2H2O; (2分)
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象即可证明,因盐酸能被高锰酸钾氧化,则选择试剂为稀硫酸、KMnO4溶液,证明炉渣中含有FeO的实验现象为稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色,
故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色;
(4)亚铁离子被高锰酸钾氧化为铁离子,根据电子得失和电荷守恒配平为5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,故答案为:5、8、MnO4-、5、Mn2+、4;
(5)FeO于稀硝酸反应的方程式可知
3FeO~NO,
3mol 22.4L
1mol V
所以
=
&;V,V=7.47L,故答案为:7.47;
(6)Fe2(SO4)3,Fe2(SO4)3的净水原理是得用铁离子的水解,生成氢氧化铁胶体,反应原理为:Fe3++3H2O?Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O?Fe(OH)3(胶体)+3H+.
| ||
(2)过量的氢氧化钠与铝离子反应生成偏铝酸根离子,方程式为Al3++4OH-═AlO2-+2H2O,故答案为:Al3++4OH-═AlO2-+2H2O; (2分)
(3)设计实验验证炉渣中含有FeO,利用酸溶液后,根据亚铁离子具有还原性,选氧化剂发生明显的现象即可证明,因盐酸能被高锰酸钾氧化,则选择试剂为稀硫酸、KMnO4溶液,证明炉渣中含有FeO的实验现象为稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色,
故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色;
(4)亚铁离子被高锰酸钾氧化为铁离子,根据电子得失和电荷守恒配平为5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,故答案为:5、8、MnO4-、5、Mn2+、4;
(5)FeO于稀硝酸反应的方程式可知
3FeO~NO,
3mol 22.4L
1mol V
所以
| 3mol |
| 1mol |
| 22.4L |
(6)Fe2(SO4)3,Fe2(SO4)3的净水原理是得用铁离子的水解,生成氢氧化铁胶体,反应原理为:Fe3++3H2O?Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O?Fe(OH)3(胶体)+3H+.
点评:本题考查铁铜及化合物的性质,氧化还原反应的配平和分析和计算,氢氧化铁的水解,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关的离子方程式或化学方程式中正确的是( )
| A、向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++HCO3-+OH-═CaCO3↓+H2O |
| B、磷酸一氢钠溶液水解:HPO42-+H2O?PO43-+H3O+ |
| C、将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol |
| D、向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
化学与生产生活密切相关.下列说法中,正确的是( )
| A、分馏、裂化、裂解是利用化学变化来炼制加工石油的三种重要方法 |
| B、蛋白质、淀粉、纤维素都能在人体内水解并提供能量 |
C、使用聚乙烯塑料制品比使用聚乳酸 (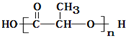 )塑料制品更环保 )塑料制品更环保 |
| D、酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对环境保护、节能减排具有重要意义 |
在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质:①FeCl3;②Fe2O3;③Cu(NO3)2;④KNO3,铜粉溶解的是( )
| A、只有①② |
| B、只有①②④ |
| C、只有①②③ |
| D、上述任意一种 |
下列事实不能用勒沙特列原理(化学平衡移动原理)解释的是( )
| A、N2+3H2?2NH3△H<0;工业上采用20MPa至50MPa的高压条件 | ||||||||
B、
| ||||||||
C、 | ||||||||
D、
|
下列物质相互反应能得到氯化镁的是( )
①镁和氯气 ②镁和盐酸 ③氧化镁和氯化铜 ④氢氧化镁和碳酸钠 ⑤氯化钡和硫酸镁.
①镁和氯气 ②镁和盐酸 ③氧化镁和氯化铜 ④氢氧化镁和碳酸钠 ⑤氯化钡和硫酸镁.
| A、全部 | B、①②⑤ |
| C、①②④⑤ | D、仅①② |
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图所示的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图所示的反应关系: