题目内容
如图所示为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图.下列说法正确的是( )
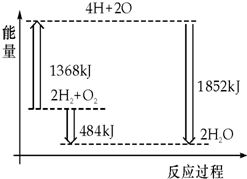

| A、H2(g)和O2(g)反应生成H2O(g),这是个吸热反应过程 |
| B、由2mol H2和1mol O2变成4mol H、2mol O原子,这是个放热反应过程 |
| C、2mol H2(g)和1mol O2(g)反应生成2mol H2O(g),共放出484kJ能量 |
| D、4mol H、2mol O生成2mol H2O(g),共放出484kJ能量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、氢气与氧气的能量比水的能量高;
B、断键需要吸收能量;
C、据图分析即可;
D、从图上可以分析出来.
B、断键需要吸收能量;
C、据图分析即可;
D、从图上可以分析出来.
解答:
解:A、氢气与氧气的能量比水的能量高,反应放热,故A错误;
B、从图上可见4mol H、2mol O原子能量高,断键吸热,故B错误;
C、从图上可知,2mol H2(g)和1mol O2(g)反应生成2mol H2O(g),共放出484kJ能量,故C正确;
D、4mol H、2mol O生成2mol H2O(g),共放出1852KJ能量,故D错误;
故选C.
B、从图上可见4mol H、2mol O原子能量高,断键吸热,故B错误;
C、从图上可知,2mol H2(g)和1mol O2(g)反应生成2mol H2O(g),共放出484kJ能量,故C正确;
D、4mol H、2mol O生成2mol H2O(g),共放出1852KJ能量,故D错误;
故选C.
点评:本题考查对图象的分析能力,分子形成原子吸热,原子组成分子放热,题目难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
等物质的量下列烃完全燃烧时,消耗氧气的量最多的是( )
| A、甲烷 |
| B、乙烯 |
| C、苯 |
| D、甲苯(C7H8) |
在两个容积相同的容器中,一个盛有C2H4气体,另一个盛有N2和CO的混合气体.在同温同压下,两容器内的气体一定具有相同的( )
①分子数 ②密度 ③质量 ④质子数⑤原子数.
①分子数 ②密度 ③质量 ④质子数⑤原子数.
| A、①④ | B、①②⑤ |
| C、④和⑤ | D、①②③ |
把0.01molNaOH分别加到下列100mL的液体中,溶液的导电能力变化不大的是( )
| A、自来水 |
| B、0.1mol/L的稀盐酸 |
| C、0.1mol/L的硫酸溶液 |
| D、0.1mol/L氯化钠溶液 |
下列溶液一定现中性的是( )
| A、PH=7的溶液 |
| B、c(H+)=10-7mol/L的溶液 |
| C、酸碱恰好完全中和的溶液 |
| D、c(H+)=c(OH-)=3.5×10-7mol/L的溶液 |
已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是( )
| A、N2H4+O2═N2+2H2O△H=-534.4kJ/mol |
| B、N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-16.7kJ/mol |
| C、N2H4(g)+O2(g)═N2(g)+2H2O(l)△H=-534.4kJ/mol |
| D、N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4kJ/mol |
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的 N2和 O2 |
| B、等体积等密度的 CO 和 N2 |
| C、等体积的 O2和 N2 |
| D、质量相等的 N2和 CO2 |