题目内容
9.下列化学用语正确的是( )| A. | CO2的结构式 O=C=O | B. | HCl的电子式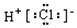 | ||
| C. | 氯离子结构示意图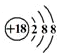 | D. | 作为相对原子质量标准的原子614C |
分析 A.二氧化碳中碳原子与2个氧原子通过共用四对电子形成共价化合物;
B.HCl属于共价化合物,不存在离子键;
C.氯离子的核电荷数为17,核外电子总数为18,最外层含有8个电子,核电荷数表示错误;
D.根据相对原子质量是以一个碳-12原子质量的$\frac{1}{12}$作为标准判断.
解答 解:A.二氧化碳为直线型结构,分子中存在两个碳氧双键,其电子式为 ,CO2的结构式为 O=C=O,故A正确;
,CO2的结构式为 O=C=O,故A正确;
B.氢原子最外层1个电子,氯原子最外层7个电子,HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物,不存在离子键,HCl电子式为 ,故B错误;
,故B错误;
C.氯元素是17号元素,故氯离子的核内质子数为17,核外电子总数为18,氯离子的结构示意图为: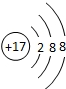 ,故C错误;
,故C错误;
D.元素左上角数字为质量数,作为相对原子质量标准的原子612C,故D错误;
故选A.
点评 本题考查了化学用语,根据结构式、电子式、结构示意图、微粒符号书写规则书写即可,注意掌握常见化学用语的书写规范,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.下列指定反应的离子方程式正确的是( )
| A. | 用过量氨水吸收工业尾气中的SO2:NH3•H2O+SO2═NH4++HSO3- | |
| B. | Ba(HCO3)2溶液中加入稀硫酸:Ba2++HCO3-+H++SO42-═BaSO4↓+CO2↑+H2O | |
| C. | FeCl2溶液中滴加过量溴水:2Fe2++Br2═2Fe3++2Br- | |
| D. | 用铜电极电解NaCl溶液:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- |
20.FeC13、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是( )
| A. | 加入KSCN溶液不一定变红色 | B. | 溶液中一定含Cu2+ | ||
| C. | 溶液中一定不含Fe3+ | D. | 剩余固体中一定是Fe |
14.不饱和内酯是各种杀菌剂、杀虫剂、高分子改性剂、医药品的原料或中间体,合成不饱和内酯已引起人们极大的兴趣.以下是利用CO2合成一种不饱和内酯的反应方程式:2Me-C≡C-Me+CO2$\stackrel{适当条件}{→}$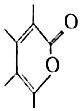 以下说法正确的是( )
以下说法正确的是( )
 以下说法正确的是( )
以下说法正确的是( )| A. | 一Me基团的电子式为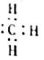 | |
| B. | 该合成过程的反应类型属于加成反应 | |
| C. | 产物与 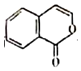 互为同分异构体 互为同分异构体 | |
| D. | 产物可与H2发生加成反应,反应的物质的量之比为1:3 |
1.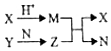 短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
 短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )| A. | 相对分子质量M>N,沸点N>M | B. | 原子半径:D>B>C>A | ||
| C. | Z为Na2CO3 | D. | 图中有两个氧化还原反应 |
18.Q、W、X、Y、Z是原子序数依次增大的短周期元素.X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z元素的原子最外层电子数相同,Z元素的原子的核电荷数是W的2倍.元素Y的合金是日常生活中使用最广泛的金属材料之一.下列说法正确的是( )
| A. | X、Y的最高价氧化物的水化物之间不能发生反应 | |
| B. | W、X两种元素形成的简单离子的半径大小顺序:X>W | |
| C. | 元素Q和Z能形成QZ2型的共价化合物 | |
| D. | Z元素的氢化物稳定性大于W元素的氢化物稳定性 |