题目内容
下表中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
| a | |||
| b | |||
| c | d | ||
| e |
| A、元素b位于ⅥA族,有+6、-2两种常见化合价 |
| B、五种元素中,元素e的性质最稳定 |
| C、原子半径有d>c>b |
| D、元素e参与形成的化合物可以作为一种半导体材料 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:a、b、c、d、e为元素周期表中前四周期的一部分元素,根据元素所在位置,可推知a为He、b为O、d为Cl、c为P、e为As.
A.氧元素没有+6价;
B.非金属性越强,氢化物越稳定;
C.同周期自左而右原子半径减小,电子层越多原子半径越大;
D.As位于金属与非金属交界处,形成的化合物可以作为一种半导体材料.
A.氧元素没有+6价;
B.非金属性越强,氢化物越稳定;
C.同周期自左而右原子半径减小,电子层越多原子半径越大;
D.As位于金属与非金属交界处,形成的化合物可以作为一种半导体材料.
解答:
解:a、b、c、d、e为元素周期表中前四周期的一部分元素,根据元素所在位置,可推知a为He、b为O、d为Cl、c为P、e为As.
A.元素b为氧,位于ⅥA族,但氧元素没有+6价,故A错误;
B.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,五种元素中As的非金属性最弱,其氢化物最不稳定,故B错误;
C.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径:c>d>b,故C错误;
D.As位于金属与非金属交界处,形成的化合物可以作为一种半导体材料,故D正确,
故选D.
A.元素b为氧,位于ⅥA族,但氧元素没有+6价,故A错误;
B.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,五种元素中As的非金属性最弱,其氢化物最不稳定,故B错误;
C.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径:c>d>b,故C错误;
D.As位于金属与非金属交界处,形成的化合物可以作为一种半导体材料,故D正确,
故选D.
点评:本题考查元素周期表与元素周期律,侧重对元素周期律的考查,注意掌握微粒半径比较及金属性、非金属性强弱比较.

练习册系列答案
相关题目
蓄电池在放电时起原电池作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电和放电时的反应:Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2则下列有关对爱迪生蓄电池的推断错误的是( )
| 放电 |
| 充电 |
| A、放电时正极附近pH增大 |
| B、充电时阴极的电极反应式为:Fe(OH)2+2e-═Fe+2OH- |
| C、放电时电解质溶液中的阴离子向正极方向移动 |
| D、蓄电池的电极可浸入某种碱性电解质溶液中 |
下列各组中互为同位素的一组是( )
| A、O2 O3 |
| B、Na2O2 Na2O |
| C、10K 10Ca |
| D、H D T |
下列各项化学语言表达正确的是( )
A、F的原子结构示意图: | ||
B、NH4Br的电子式: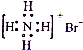 | ||
C、原子核内有l8个中子的氯原子:
| ||
| D、乙烯的结构简式:CH2CH2 |
几种短周期元素的原子半径及主要化合价如下表,下列叙述不正确的是( )
元素代号 | X | Y | Z | W | T |
| 原子半径/nm | 0.186 | 0.143 | 0.102 | 0.074 | 0.071 |
| 主要化合价 | +1 | +3 | +6、-2 | -2 | -1、无正价 |
| A、Y、X的最高价氧化物的水化物之间能反应 |
| B、Z的氢化物与T的单质具有相同的核外电子数 |
| C、X与W形成的化合物中都只含离子键 |
| D、Z的氧化物不止一种 |
下列四个数据都表示合成氨的反应速率,N2+3H2?2NH3,其中代表同一反应速率的是( )
①v(N2)=0.03mol?L-1?min-1 ②v(NH3)=0.09mol?L-1?min-1
③v(H2)=0.045mol?L-1?min-1 ④v(H2)=0.135mol?L-1?min-1.
①v(N2)=0.03mol?L-1?min-1 ②v(NH3)=0.09mol?L-1?min-1
③v(H2)=0.045mol?L-1?min-1 ④v(H2)=0.135mol?L-1?min-1.
| A、①② | B、①③ | C、③④ | D、②④ |
现有NaOH、Na2CO3和Ba(OH)2三种无色溶液,选用下列一种试剂,一次即可鉴别的是( )
| A、CuCl2溶液 |
| B、稀硫酸 |
| C、FeCl3溶液 |
| D、CO2 |
