题目内容
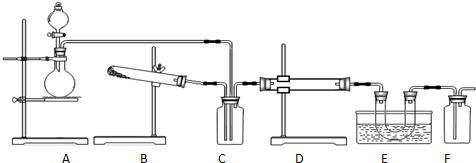
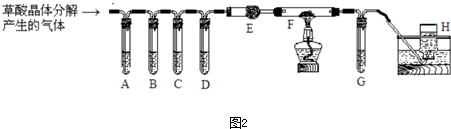
乙二酸俗称草酸,在工业中有重要作用,可用来除锈,具有还原性和不稳定性,加热会分解生成三种氧化物.两个学习小组用如图装置探究乙二酸(HOOC-COOH)受热分解的部分产物.
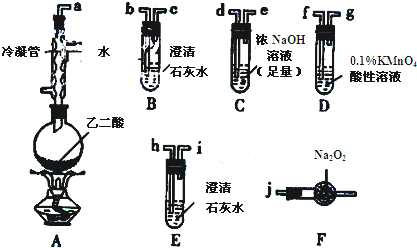
(1)甲组:
①按接口顺序:a-b-c-d-e-f-g-h连接装置进行实验.B中溶液变浑浊,证明分解产物中有 ;装置C的作用是 ;E中溶液变浑浊,D中的现象是 ,证明分解产物中有 ;
②乙二酸受热分解的化学方程式为 .
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要反应的化学方程式为 ;
②从A~F中选用装置进行实验,证明甲组通入D的气体能否与Na2O2反应.最简单的装置接口连接顺序是 ;实验后用F中的固体进行验证的方法是 (可另选试剂);
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+.该反应的离子方程式是: .

(1)甲组:
①按接口顺序:a-b-c-d-e-f-g-h连接装置进行实验.B中溶液变浑浊,证明分解产物中有
②乙二酸受热分解的化学方程式为
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要反应的化学方程式为
②从A~F中选用装置进行实验,证明甲组通入D的气体能否与Na2O2反应.最简单的装置接口连接顺序是
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+.该反应的离子方程式是:
考点:性质实验方案的设计
专题:实验设计题
分析:(1)①用澄清石灰水检验二氧化碳;用氢氧化钠溶液吸收多余的二氧化碳;再用酸性高锰酸钾溶液检验CO;
②乙二酸受热分解生成二氧化碳、一氧化碳和水;
(2)①二氧化碳与过氧化钠反应生成碳酸钠和氧气;
②要检验CO能否与Na2O2反应,需要先除去CO2;检验F中的固体是否含有碳酸钠,可以用稀硫酸检验;
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+,Na2C2O4被氧化为二氧化碳.
②乙二酸受热分解生成二氧化碳、一氧化碳和水;
(2)①二氧化碳与过氧化钠反应生成碳酸钠和氧气;
②要检验CO能否与Na2O2反应,需要先除去CO2;检验F中的固体是否含有碳酸钠,可以用稀硫酸检验;
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+,Na2C2O4被氧化为二氧化碳.
解答:
解:(1)①用澄清石灰水检验二氧化碳,所以混合气体进入澄清石灰水,若B中石灰水变浑浊,说明分解产物中含有CO2;然后用氢氧化钠溶液吸收多余的二氧化碳;再用酸性高锰酸钾溶液检验CO,若酸性高锰酸钾溶液褪色,说明含有CO;
故答案为:CO2;除去CO2;溶液褪色;CO;
②乙二酸受热分解生成二氧化碳、一氧化碳和水,则分解的方程式为:H2C2O4
CO2↑+CO↑+H2O;故答案为:H2C2O4
CO2↑+CO↑+H2O;
(2)①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,发生的反应是二氧化碳与过氧化钠反应生成碳酸钠和氧气,则主要反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2;
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
②要检验CO能否与Na2O2反应,需要先除去CO2,所以混合气体,要先通过足量的氢氧化钠溶液,然后通过过氧化钠,则仪器连接顺序为:a-d-e-j;检验F中的固体是否含有碳酸钠,可以用稀硫酸检验,检验操作为:取少量F中的固体于试管中,加入适量稀硫酸,将生成的气体通入澄清石灰水中,若溶液变浑浊,则发生了反应,若不变浑浊,则未发生反应;
故答案为:a-d-e-j;取少量F中的固体于试管中,加入适量稀硫酸,将生成的气体通入澄清石灰水中,若溶液变浑浊,则发生了反应,若不变浑浊,则未发生反应;
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+,Na2C2O4被氧化为二氧化碳,其反应的离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
故答案为:CO2;除去CO2;溶液褪色;CO;
②乙二酸受热分解生成二氧化碳、一氧化碳和水,则分解的方程式为:H2C2O4
| ||
| ||
(2)①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,发生的反应是二氧化碳与过氧化钠反应生成碳酸钠和氧气,则主要反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2;
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
②要检验CO能否与Na2O2反应,需要先除去CO2,所以混合气体,要先通过足量的氢氧化钠溶液,然后通过过氧化钠,则仪器连接顺序为:a-d-e-j;检验F中的固体是否含有碳酸钠,可以用稀硫酸检验,检验操作为:取少量F中的固体于试管中,加入适量稀硫酸,将生成的气体通入澄清石灰水中,若溶液变浑浊,则发生了反应,若不变浑浊,则未发生反应;
故答案为:a-d-e-j;取少量F中的固体于试管中,加入适量稀硫酸,将生成的气体通入澄清石灰水中,若溶液变浑浊,则发生了反应,若不变浑浊,则未发生反应;
(3)硫酸酸化的KMnO4溶液能与Na2C2O4反应生成Mn2+,Na2C2O4被氧化为二氧化碳,其反应的离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
点评:本题考查了物质性质实验方案设计,涉及物质的检验、方程式的书写、实验操作设计等,题目难度中等,侧重于考查学生的实验探究能力和对基础知识的综合应用能力.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列反应属于加成反应的是( )
| A、甲烷与氯气的混合气体在光照条件下的反应 |
| B、丙烯和氯气在一定条件下生成ClCH2CH=CH2的反应 |
| C、乙烯使酸性高锰酸钾溶液褪色的反应 |
| D、乙烯与溴水的反应 |
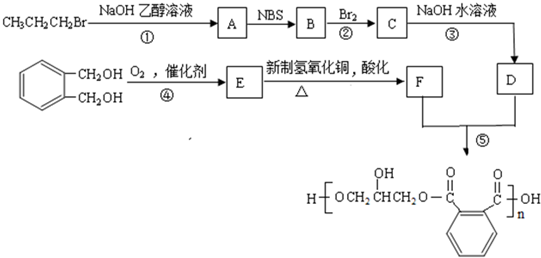
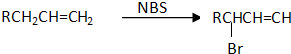
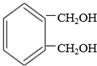 互为同分异构体的结构简式
互为同分异构体的结构简式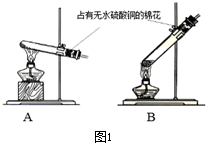
 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题.该小组设计的简单实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题.该小组设计的简单实验装置如图所示: