题目内容
11.根据晶体的性质判断下列哪种晶体最有可能是分子晶体( )| A. | Al4C3晶体,熔点2200℃,熔融态不导电 | |
| B. | C3N4晶体具有比金刚石还大的硬度 | |
| C. | VF5晶体易溶于一些有机溶剂中 | |
| D. | BaCl2熔融状态下能够导电 |
分析 A.熔点高不是分子晶体的性质;
B.硬度大是原子晶体的性质;
C.熔沸点较低,易溶于有机溶剂;
D.熔融时能导电,分子晶体构成微粒为分子,不可能电离,不导电.
解答 解:A.碳化铝,黄色晶体,熔点2200℃,熔融态不导电,应为原子晶体,故A错误;
B.C3N4晶体具有比金刚石还大的硬度,属于原子晶体,故B错误;
C.五氟化钒,易溶于有机溶剂中,具有分子晶体的性质,属于分子晶体,故C正确;
D.BaCl2熔融状态下能够导电,应为离子晶体或金属晶体,故D错误;
故选C.
点评 本题考查原子晶体、分子晶体、离子晶体的性质,熟悉熔沸点及构成微粒是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
12.如图是元素周期表中短周期的一部分,若A原子最外层的电子数比次外层少3,则下列说法正确的是( ) 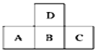

| A. | 只有A的单质存在同素异形体 | |
| B. | D的最高正价与B的最高正价相等 | |
| C. | A、B、C的最高价氧化物对应水化物的酸性强弱的关系是C>B>A | |
| D. | 原子半径的大小顺序是C>B>A>D |
10.X、Y、Z三者均为短周期元素,已知X元素有一种同位素不含中子,Y元素原子的最外层电子数是次外层电子数的2倍,Z元素原子的最外层电子数是次外层电子数的3倍.下列化学式①XYZ3②X2YZ2③X2YZ3④X2Y2Z2⑤X2Y2Z4⑥X4Y2Z2中,并非都存在的一组分子是( )
| A. | ①② | B. | ④⑥ | C. | ③⑤ | D. | ②④ |
3.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | NO2和N2O4平衡混合气缩小体积加压后颜色变深 | |
| C. | 硫酸工业上SO2氧化成SO3,宜采用空气过量 | |
| D. | 煅烧硫铁矿利于SO2的生成 |
1.下列说法正确的是( )
| A. | 分子中含有羟基的物质溶于水后,溶液一定显酸性 | |
| B. | 丙酸、乙酸甲酯、甲酸乙酯互为同分异构体 | |
| C. | 能发生银镜反应的一定是醛 | |
| D. | 乙醇发生酯化反应断裂碳氧键而失去羟基 |
 ④在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为7NA.
④在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为7NA. 肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.