题目内容
6.已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为283 kJ | |
| B. | 两个反应都只发生了共价键的断裂和形成 | |
| C. | CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移数为6.02×1023 | |
| D. | Na2O2(s)+CO(g)═Na2CO3(s)△H=-509 kJ/mol. |
分析 A.燃烧热单位为kJ/mol;
B.过氧化钠存在离子键和共价键;
C.CO2(g)与Na2O2(s)反应放出452kJ热量时,说明2mol过氧化钠参加反应;
D.根据盖斯定律利用题给热化学方程式合并消去二氧化碳得到热化学方程式.
解答 解:A.燃烧热单位为kJ/mol,故A错误;
B.过氧化钠存在离子键和共价键,还存在离子键的断裂和形成,故B错误;
C.CO2(g)与Na2O2(s)反应放出452kJ热量时,说明2mol过氧化钠参加反应,则转移2mol电子,故C错误;
D.已知:①2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol ②Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ•mol-1,根据盖斯定律合并热化学方程式得到,$\frac{①+②×2}{2}$得到的热化学方程式为 CO(g)+Na2O2(s)=2Na2CO3(s);△H=-509kJ/mol,故D正确.
故选D.
点评 本题考查较为综合,为高考常见题型和高频考点,题目涉及热化学方程式的书写判断,燃烧热的概念应用,反应焓变的意义,盖斯定律的应用,难度中等,注意把握盖斯定律的运用.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
16.有机物C5H11OH为饱和一元醇,其可能的结构共有( )
| A. | 3种 | B. | 5种 | C. | 8种 | D. | 9种 |
14.实验是研究化学的基础,下列有关实验的方法、装置或操作不正确的是( )
| A. |  从氯化钠溶液中得到氯化钠晶体,可使用如图甲所示实验装置 | |
| B. |  分离石油,得到汽油、煤油和柴油等各种馏分,可使用如图乙所示实验装置 | |
| C. |  实验室制氨气,实验装置如图丙所示 | |
| D. |  分离乙醇和乙酸的混合液,实验装置如图丁所示 |
1.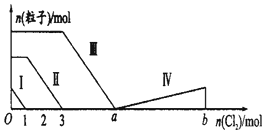 向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )
 向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法不正确的是( )| A. | 线段Ⅲ表示Br-的变化情况 | B. | 原溶液中n(FeI2):n(FeBr2)=1:3 | ||
| C. | 线段Ⅳ表示IO4-的变化情况 | D. | 根据图象可以计算a的值为6 |
18.下列分离或提纯物质的方法正确的是( )
| A. | 用酒精萃取碘水中的碘 | |
| B. | 用蒸馏法进行海水淡化 | |
| C. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| D. | 用加热-蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
15.由重水D2O组成的水,D2O的离子积为1.6×10-15,可用PH一样定义规定PD=-lg{c(D+)},下列关于PD的叙述,正确的是( )
| A. | D2O呈中性,PD=7 | |
| B. | 1LD2O溶液中含0.01molNaOD,PD=12 | |
| C. | 用D2O溶解0.1molDCl成1L溶液,PD=2 | |
| D. | 在100ml0.25mol/LDCl溶液中加入50ml0.2mol/L的NaOD的D2O溶液,PD=1 |