题目内容
20.下列鉴别或者除杂方法可行的是( )| A. | 用水鉴别甲酸、乙醛、乙酸 | |
| B. | 除去乙烷中少量的乙烯:光照条件下通入氢气 | |
| C. | 除去乙醇中少量的乙酸:加入足量的生石灰,过滤 | |
| D. | 用燃烧的方法鉴别乙醇、苯和四氯化碳 |
分析 A.甲酸、乙醛、乙酸均溶于水;
B.乙烯与氢气发生加成反应,但乙烷中可引入新杂质氢气;
C.乙酸与CaO反应后,增大与乙醇的沸点差异;
D.乙醇燃烧有淡蓝色火焰,苯燃烧冒黑烟,四氯化碳不能燃烧.
解答 解:A.甲酸、乙醛、乙酸均溶于水,则水不能鉴别,故A错误;
B.乙烯与氢气发生加成反应,但乙烷中可引入新杂质氢气,不能除杂,应选溴水、洗气,故B错误;
C.乙酸与CaO反应后,增大与乙醇的沸点差异,不能过滤,应选蒸馏法分离,故C错误;
D.乙醇燃烧有淡蓝色火焰,苯燃烧冒黑烟,四氯化碳不能燃烧,则燃烧法可鉴别,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、物质的鉴别、混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意有机物性质及实验评价的结合,题目难度不大.

练习册系列答案
相关题目
10.中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
Ⅰ.改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气.
(1)已知:H2(g)+1/2O2(g)═H2O(g)△H1=-241.8kJ•mol-1
2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
由此可知焦炭与水蒸气反应的热化学方程式为C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
(2)煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-
(已知:H2S:Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11)
(3)现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中发生如表反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H,得到两组数据
该反应的△H<0(填“<”或“>”);若在9000C时,另做一组实验,在2L的恒容密闭容器中加入l0mol CO,5mo1H2O,2mo1CO2,5mol H2,则此时?正<?逆(填“<”,“>”,“=”).
(4)一定条件下,某密闭容器中已建立A(g)+B(g)?C(g)+D(g)△H>0的化学平衡,其时间速率图象如图1,下列选项中对于t1时刻采取的可能操作及其平衡移动情况判断正确的是A
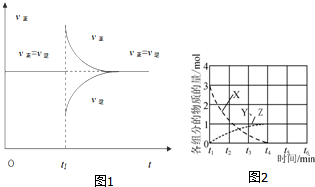
A.减小压强,同时升高温度,平衡正向移动
B.增加B(g)浓度,同时降低C(g)浓度,平衡不移动
C.增加A(g)浓度,同时降低温度,平衡不移动
D.保持容器温度压强不变通入稀有气体,平衡不移动
Ⅱ.压缩天然气(CNG)汽车的优点之一是利用催化技术将NOx转变成无毒的CO2和N2.
①CH4(g)+4NO(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H1<0
②CH4(g)+2NO2(g)$\stackrel{催化剂}{?}$(g)+CO2(g)+2H2O(g)△H2<0
(5)收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V (NO):V (NO2)=1:1.
(6)在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图2所示.写出Y和Z的化学式:N2O、NO2.
Ⅰ.改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气.
(1)已知:H2(g)+1/2O2(g)═H2O(g)△H1=-241.8kJ•mol-1
2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
由此可知焦炭与水蒸气反应的热化学方程式为C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
(2)煤气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为CO32-+H2S=HCO3-+HS-
(已知:H2S:Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11)
(3)现将不同量的CO(g)和H2O(g)分别通人到体积为2L的恒容密闭容器中发生如表反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H,得到两组数据
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡 所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
(4)一定条件下,某密闭容器中已建立A(g)+B(g)?C(g)+D(g)△H>0的化学平衡,其时间速率图象如图1,下列选项中对于t1时刻采取的可能操作及其平衡移动情况判断正确的是A

A.减小压强,同时升高温度,平衡正向移动
B.增加B(g)浓度,同时降低C(g)浓度,平衡不移动
C.增加A(g)浓度,同时降低温度,平衡不移动
D.保持容器温度压强不变通入稀有气体,平衡不移动
Ⅱ.压缩天然气(CNG)汽车的优点之一是利用催化技术将NOx转变成无毒的CO2和N2.
①CH4(g)+4NO(g)$\stackrel{催化剂}{?}$2N2(g)+CO2(g)+2H2O(g)△H1<0
②CH4(g)+2NO2(g)$\stackrel{催化剂}{?}$(g)+CO2(g)+2H2O(g)△H2<0
(5)收集某汽车尾气经测量NOx的含量为1.12%(体积分数),若用甲烷将其完全转化为无害气体,处理1×104L(标准状况下)该尾气需要甲烷30g,则尾气中V (NO):V (NO2)=1:1.
(6)在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图2所示.写出Y和Z的化学式:N2O、NO2.
11.下列有关实验装置或实验操作正确的是( )
| A. | 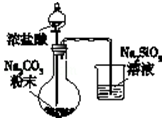 验证酸性:H2CO3>H2SiO3 | |
| B. | 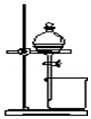 用于分离CCl4萃取碘水后的有机层和水层 | |
| C. | 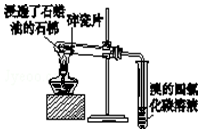 证明石蜡油分解生成的气体是乙烯 | |
| D. | 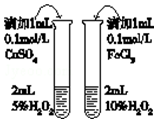 比较不同催化剂对反应速率的影响 |
12.下列物质其结构具有正四面体构型的是( )
①乙烷、②CHCl3、③甲烷、④四氯化碳、⑤白磷(P4)
①乙烷、②CHCl3、③甲烷、④四氯化碳、⑤白磷(P4)
| A. | ①②③ | B. | ③④⑤ | C. | ①④⑤ | D. | ②③④ |
9.在恒容密闭容器中通入X并发生反应:2X(g)?Y(g),温度T1、T2下Y的物质的量浓度c(Y)随时间t变化的曲线如图所示,下列叙述正确的是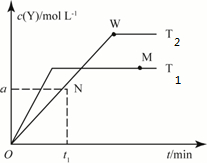 ( )
( )
 ( )
( )| A. | T2下,在0~t1时间内v(X)=$\frac{a}{{t}_{1}}$mol•L-1•min-1 | |
| B. | N点时气体的总压强大于W点时气体的总压强 | |
| C. | M点的正反应速率小于N点的逆反应速率 | |
| D. | W点时再加入一定量Y,平衡后X的转化率减小 |
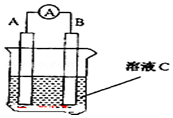 如图原电池装置图:
如图原电池装置图: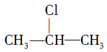 +NaOH$→_{△}^{醇}$CH3-CH═CH2+NaCl+H2O,
+NaOH$→_{△}^{醇}$CH3-CH═CH2+NaCl+H2O,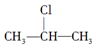 $→_{-NaCl,-H_{2}O}^{NaOH、醇、△}$CH3-CH═CH2下面是几种有机化合物的转化关系:
$→_{-NaCl,-H_{2}O}^{NaOH、醇、△}$CH3-CH═CH2下面是几种有机化合物的转化关系: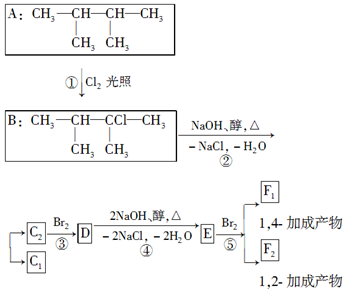
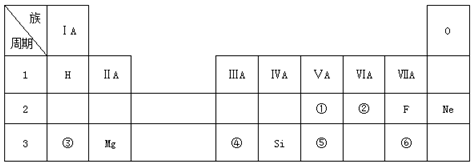
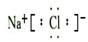 .
.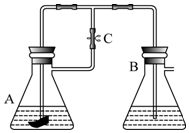 另外还有一种方法制备Fe(OH)2.在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备.在锥形瓶B中加入的试剂是氢氧化钠溶液.这样生成的Fe(OH)2沉淀也能较长时间保持白色,理由是A中反应生成的氢气,充满了整个实验装置,外界空气不易进入.
另外还有一种方法制备Fe(OH)2.在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备.在锥形瓶B中加入的试剂是氢氧化钠溶液.这样生成的Fe(OH)2沉淀也能较长时间保持白色,理由是A中反应生成的氢气,充满了整个实验装置,外界空气不易进入.