题目内容
18.下列变化的实质相似的是( )| A. | 浓硫酸与浓盐酸在空气中敞口放置时浓度均减小 | |
| B. | 金属导电与电解质溶液导电 | |
| C. | 在净水过程中分别使用明矾和漂白粉 | |
| D. | 工业上制取金属铁和金属铜 |
分析 A.浓硫酸具有吸水性、浓盐酸具有挥发性;
B.金属含有自由移动的电子能导电,电解质溶液含有自由移动的阴阳离子能导电;
C.明矾没有强氧化性,漂白粉有强氧化性;
D.金属铁和铜制备是化合态变化为游离态.
解答 解:A.浓硫酸具有吸水性,能吸收空气中的水分而使其溶液浓度减小,浓盐酸具有挥发性,能挥发导致溶液浓度降低,所以二者原理不同,故A错误;
B.金属单质靠电子导电,电解质靠自由移动的阴阳离子导电,金属与电解质溶液的导电微粒不相同,故B错误;
C.明矾中的铝离子在水中水解生成氢氧化铝胶体,能吸附悬浮颗粒,而净水,漂白粉有强氧化性,能杀死水中的细菌和病毒,所以二者作用原理不同,故C错误;
D.工业上制取金属铁是利用还原剂还原金属氧化物得到,制备金属铜可以利用铁还原铜离子生成单质铜,反应都是氧化还原反应,故D正确;
故选D.
点评 本题考查了物质性质、物质制备、物质应用的原理分析判断,注意知识的积累,题目难度不大.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
6.用石墨电极电解CuCl2溶液(装置如图所示),下列相关分析正确的是( )
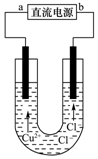

| A. | a端是直流电源的正极 | |
| B. | 阴极上发生的反应:Cu2++2e-=Cu | |
| C. | 通电使CuCl2发生电离 | |
| D. | 通电一段时间后,在阴极附近观察到黄绿色气体 |
9.已知还原性SO32->I-.某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向该无色溶液中滴加少量溴水,溶液仍呈无色.下列关于该溶液的判正确的是( )
| A. | 肯定不含I- | B. | 肯定含有Na+ | ||
| C. | 肯定不含SO42-肯定含有SO32- | D. | 不能肯定是否含有SO42 |
6. 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )| A. | a 电极发生反应:H2NCH2CH2NH2+16e-+4H2O═2CO2↑+N2↑+16H+ | |
| B. | 质子交换膜处H+由右向左移动 | |
| C. | 该电池在微生物作用下将化学能转化为电能 | |
| D. | 开始放电时b极附近pH不变 |
13.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 50mL18mol•L-1浓硫酸与足量铜供热,转移电子数为0.9NA | |
| C. | 0.1molCl2通入含0.1molFeBr2溶液中,被氧化的溴离子数为0.2NA | |
| D. | 标准状况下,2.24LNO和足量O2反应生成物中含有NO2分子数为0.1NA |
3.下列物质的性质与应用对应关系正确的是( )
| A. | 氢氟酸具有弱酸性,可用作玻璃蚀刻剂 | |
| B. | 干冰气化时吸热,可用作制冷剂 | |
| C. | 钠与水反应,可用于除去乙醇中少量的水 | |
| D. | 硅酸钠易溶于水,可用作木材防火剂 |
10.某柔性燃料电池(以甲醇为燃料,酸性介质)结构示意如图.下列有关说法正确的是( )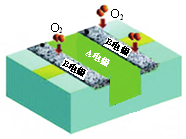

| A. | 电池工作时,电子由A电极经外电路流向B电极 | |
| B. | 电池工作时,减少的化学能完全转化为电能 | |
| C. | A电极发生的电极反应为:CH3OH-6e-+H2O═CO2+6H+ | |
| D. | B电极每消耗1 mol O2,电池中减少4 mol H+ |
8.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含有大量Fe3+的溶液中:Na+、Fe2+、Br-、SO42- | |
| B. | 1.0 mol/L KMnO4的溶液中:H+、Na+、Cl-、SO42- | |
| C. | 能与铝反应放出H2的溶液中:K+、Mg2+、SO42-、NO3- | |
| D. | 水电离的c(H+)和C(OH-)之积为l×l0-20mol2•L-2的溶液中:Na+、K+、CO32-、Cl- |