题目内容
在密闭容器中发生下列反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是( )
| A、A的转化率变大 |
| B、平衡向正反应方向移动 |
| C、D的体积分数变大 |
| D、a<c+d |
考点:化学平衡的计算
专题:
分析:先判断气体体积刚压缩平衡还未移动时D的浓度与原来浓度的关系,再与再次达到平衡时D的浓度作比较判断平衡如何移动,从而判断各选项是否正确.
解答:
解:气体体积刚压缩平衡还未移动时D的浓度是原来的2倍,当再次达到平衡时,D的浓度为原平衡的1.5倍,D的浓度减小,所以压缩体积使平衡向逆反应方向移动.
A、平衡向逆反应方向移动,A的转化率变小,故A错误;
B、平衡向逆反应方向移动,故B错误;
C、平衡向逆反应方向移动,D的体积分数减小,故C错误;
D、增大压强,平衡向气体体积减小的方向移动,该平衡向逆反应方向移动,所以a<c+d,故D正确.
故选D.
A、平衡向逆反应方向移动,A的转化率变小,故A错误;
B、平衡向逆反应方向移动,故B错误;
C、平衡向逆反应方向移动,D的体积分数减小,故C错误;
D、增大压强,平衡向气体体积减小的方向移动,该平衡向逆反应方向移动,所以a<c+d,故D正确.
故选D.
点评:正确判断气体体积刚压缩的一瞬间D的浓度是解本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图所示,若关闭Ⅰ阀,打开Ⅱ阀,让潮湿的氯气经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色.甲瓶中所盛的试剂不可能是 ( )
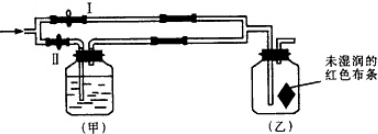

| A、浓H2SO4 |
| B、NaCl溶液 |
| C、Ba(OH)2溶液 |
| D、NaOH溶液 |
将a mol氮气和b mol氢气及c mol氨气混合充入一密闭容器中反应,在一定条件下到达平衡时,测知容器内氨气为x mol 这x的取值为( )
| A、c+2a | ||
B、
| ||
| C、0<x<c | ||
| D、c<x<c+2a |
荧光素(X)常用于钞票等防伪印刷,下列关于它的说法正确的是( )
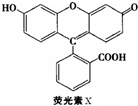

| A、荧光素的分子式为C20H14O5 |
| B、1molX最多能与9mol氢气反应 |
| C、1molX与足量的浓溴水反应,最多消耗4molBr2 |
| D、X能与甲醛发生缩聚反应 |