题目内容
 一种碳纳米管能够吸附氢气,可做充电电池(如图所示)的碳电极,该电池的电解质为6mol/L KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,可做充电电池(如图所示)的碳电极,该电池的电解质为6mol/L KOH溶液,下列说法中正确的是( )| A、充电时将碳电极与电源的正极相连 |
| B、充电时阴极发生氧化反应 |
| C、放电时镍电极反应为:NiO(OH)+H2O+e-═Ni(OH)2+OH- |
| D、放电时碳电极反应为:2H--2e-═H2 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:充电时,该装置是电解池,阴极上得电子发生还原反应,阳极上失电子发生氧化反应;放电时,该装置是原电池,正极上得电子发生还原反应,负极上失电子发生氧化反应.
解答:
解:A.充电时,碳电极与电源的负极相连,故A错误;
B.充电时,阴极上得电子发生还原反应,故B错误;
C.放电时,正极上得电子发生还原反应,电极反应式为:NiO(OH)+H2O+e-=Ni(OH)2+OH-,故C正确;
D.放电时,碳电极上失电子发生氧化反应,电极反应式为:H2+2OH--2e-=2H2O,故D错误;
故选C.
B.充电时,阴极上得电子发生还原反应,故B错误;
C.放电时,正极上得电子发生还原反应,电极反应式为:NiO(OH)+H2O+e-=Ni(OH)2+OH-,故C正确;
D.放电时,碳电极上失电子发生氧化反应,电极反应式为:H2+2OH--2e-=2H2O,故D错误;
故选C.
点评:本题考查原电池和电解池原理,电极反应式的书写是学习难点,易错选项是D,要注意结合电解质溶液的酸碱性书写电极反应式,题目难度不大.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
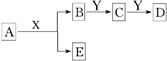 中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去).下列推断正确的是( )
中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去).下列推断正确的是( )| A、若A是CaC2,X是H2O,则Y一定是溴水 |
| B、若A是金属钠,X是H2O,则E一定能还原Fe2O3 |
| C、若Y是NaOH,C是白色沉淀,则A与X一定发生置换反应 |
| D、若Y是氧气,D是氧化物,则A与X一定发生氧化还原反应 |
下列关于盐类水解的叙述中,错误的是( )
| A、盐类水解是中和反应的逆反应 |
| B、盐类水解过程是吸热过程 |
| C、含有弱酸根盐的水溶液一定显碱性 |
| D、盐溶液的酸碱性主要决定于形成盐的酸和碱的相对强弱 |
将相对分子质量为M 的某气体VL(标准状况下)溶于10mL水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为( mol/L)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
把M mol H2和N mol C2H4混合,在一定条件下使它们一部分发生反应生成W mol C2H6,将反应后的混合气体完全燃烧,消耗氧的物质的量为( )
| A、M+3N | ||||
B、
| ||||
C、
| ||||
D、
|
下列说法中正确的是( )
| A、伴有能量变化的物质变化都是化学变化 |
| B、放热反应在常温下一定很容易发生 |
| C、吸热反应只有在点燃条件下才能发生 |
| D、反应是吸热还是放热是由反应物和生成物所具有的总能量的相对大小而决定的 |
室温下,0.1mol?L-1 CH3COONa溶液与0.1mol?L-1 NaCl溶液等体积混合(忽略溶液体积变化),下列有关叙述正确的是( )
| A、混合前CH3COONa溶液中由水电离出来的c(OH-)>1×10-7mol?L-1 |
| B、混合前NaCl溶液中:c(Na+)+c(OH-)=c(Cl-)+c(H+) |
| C、混合溶液中:c(Cl-)>c(CH3COOH)>c(OH-) |
| D、混合溶液中:c(Cl-)+c(CH3COO-)=0.1mol?L-1 |
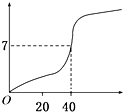 用1.0mol/L的NaOH溶液中和某浓度的H2SO4溶液,其水溶液的pH和所用NaOH溶液的体积关系变化如图所示,则原H2SO4溶液的物质的量浓度和完全反应后溶液的大致体积是( )
用1.0mol/L的NaOH溶液中和某浓度的H2SO4溶液,其水溶液的pH和所用NaOH溶液的体积关系变化如图所示,则原H2SO4溶液的物质的量浓度和完全反应后溶液的大致体积是( )| A、1.0mol/L,20mL |
| B、0.5mol/L,40mL |
| C、0.5mol/L,80mL |
| D、1.0mol/L,80mL |
