题目内容
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 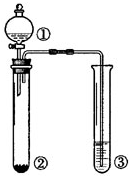 |
| A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A、A | B、B | C、C | D、D |
考点:实验装置综合
专题:实验评价题
分析:A.二氧化锰与浓盐酸反应需要加热;
B.浓硫酸具有脱水性及强氧化性,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr;
C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡;
D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应.
B.浓硫酸具有脱水性及强氧化性,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr;
C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡;
D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应.
解答:
解:A.二氧化锰与浓盐酸反应需要加热,图中缺少加热装置,故A错误;
B.蔗糖与浓硫酸混合,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr,则由实验可知浓硫酸具有脱水性、氧化性,故B正确;
C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡,则结论不合理,如二氧化硫与氯化钡不反应,故C错误;
D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应,则不能比较酸性碳酸>硅酸,故D错误;
故选B.
B.蔗糖与浓硫酸混合,蔗糖脱水得到C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应生成硫酸和HBr,则由实验可知浓硫酸具有脱水性、氧化性,故B正确;
C.稀盐酸与亚硫酸钠生成二氧化硫,在③中二氧化硫与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡,则结论不合理,如二氧化硫与氯化钡不反应,故C错误;
D.浓硝酸易挥发,则③中可能发生硝酸与硅酸钠的反应,则不能比较酸性碳酸>硅酸,故D错误;
故选B.
点评:本题考查实验装置的综合应用,为高频考点,涉及物质的制备、酸性比较、氧化还原反应等,把握实验装置的作用为解答的关键,侧重分析、实验能力的考查,题目难度中等.

练习册系列答案
相关题目
向200ml 0.1mol/L的FeCl2溶液中加入适量的NaOH溶液,使Fe2+恰好完全沉淀,过滤,小心加热沉淀,直到水分蒸干,再灼烧到质量不再变化,此时固体的质量为( )
| A、1.14g | B、1.6g |
| C、2.82g | D、4.36g |
关于有机物结构、性质、鉴别的叙述正确的是( )
| A、淀粉和纤维素都是多糖,其分子式为 (C6H10O5)n |
| B、乙烯和苯都能使溴水褪色,故不能用溴水鉴别乙烯和苯蒸气 |
| C、NH4Cl可以使蛋白质变性形成沉淀从溶液中析出 |
| D、苯与酸性KMnO4溶液混合振荡、静置分层,下层液体为无色 |
将氯化钠、乙醇、碘分别从以下三种混合物中分离出来,①食盐水②乙醇溶液③碘水( )
| A、蒸馏、萃取、蒸发 |
| B、萃取、蒸馏、蒸发 |
| C、蒸发、萃取、蒸馏 |
| D、蒸发、蒸馏、萃取 |
金属镁的密度较小,镁合金的强度高、机械性能好,是制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.从化学原理和经济效益角度分析,下列海水中提取镁的方法最合理的是( )
A、海水
| |||||||||||
B、海水
| |||||||||||
C、海水
| |||||||||||
D、海水
|
把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是( )
| A、H2SO4溶液 |
| B、Na2SO4溶液 |
| C、Na2CO3溶液 |
| D、FeC13溶液 |
下列关于热化学反应的描述中正确的是( )
A、葡萄糖的燃烧热是2800 kJ?mol-1,则
| ||
B、燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+
则CH3OH(g)的燃烧热为192.9 kJ?mol-1 | ||
| C、H2(g)的燃烧热是285.8 kJ?mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
| D、已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ?mol-1 |
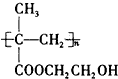 制成超薄镜片,其合成路线可以是:
制成超薄镜片,其合成路线可以是:
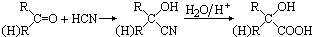
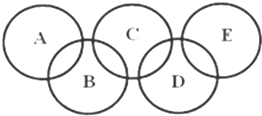 如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: