题目内容
物质的分类方法有:交叉分类法、树状分类法等多种方法,下列对无机化合物分类如图: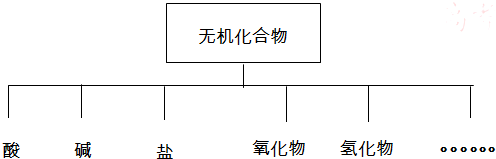
(1)如图所示的物质分类方法名称是 .
(2)以K、Na、H、O、S、N等元素组成合适的物质,分别填在下表中②、④、⑥后面.
(3)写出⑦与过量的③溶液反应的离子方程式 .

(1)如图所示的物质分类方法名称是
(2)以K、Na、H、O、S、N等元素组成合适的物质,分别填在下表中②、④、⑥后面.
| 物质类别 | 强酸 | 强碱 | 酸式盐 | 氧化物 | 氢化物 |
| 化学式 | ①HNO3 ② | ③NaOH ④ | ⑤NaHSO4 ⑥ | ⑦SO2 ⑧SO3 | ⑨NH3 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树;
(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠;
(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠;
解答:
解:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,
故答案为:树状分类法;
(2)酸电离出的阳离子全部是氢离子的化合物,如H2SO4;碱电离出的阴离子全部为氢氧根离子,如KOH;盐电离出得阳离子为金属离子,阴离子为酸根离子,如KHSO3(或钠盐、铵盐)、KHS(或钠盐、铵盐)、KHSO4 (或铵盐);
故答案为:②H2SO4;④KOH;⑥KHSO3(或钠盐、铵盐)、KHS(或钠盐、铵盐)、KHSO4 (或铵盐);
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠,其反应的离子方程式为:SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
故答案为:树状分类法;
(2)酸电离出的阳离子全部是氢离子的化合物,如H2SO4;碱电离出的阴离子全部为氢氧根离子,如KOH;盐电离出得阳离子为金属离子,阴离子为酸根离子,如KHSO3(或钠盐、铵盐)、KHS(或钠盐、铵盐)、KHSO4 (或铵盐);
故答案为:②H2SO4;④KOH;⑥KHSO3(或钠盐、铵盐)、KHS(或钠盐、铵盐)、KHSO4 (或铵盐);
(3)二氧化硫和氢氧化钠反应生成水和亚硫酸钠,其反应的离子方程式为:SO2+2OH-═SO32-+H2O,故答案为:SO2+2OH-═SO32-+H2O;
点评:本题考查物质的分类、氧化还原反应、化学方程式和离子方程式的书写等,题目难度不大,注意把握相关概念.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入1L的密闭容器中发生反应:CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如下表:下列说法正确的是( )
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如下表:下列说法正确的是( )
| 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A、T1>T2,且a>0 |
| B、当温度为T2、反应进行到40 min时,x>0.15 |
| C、温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol |
| D、温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,ν(正)>ν(逆) |
下列属于放热反应的是( )
| A、浓硫酸的稀释 |
| B、铝热反应 |
| C、氢气还原氧化铜 |
| D、Ba(OH)2?2H2O和NH4Cl(固体)混合 |
下列有关化学用语表示正确的是( )
A、氮气的电子式: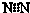 | ||
B、羟基的电子式: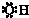 | ||
C、氯离子的结构示意图: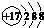 | ||
D、质子数为92、中子数为146的铀(U)原子的核素符号:
|
下列有机反应中,有一项反应类型不同于其他三项的是( )
A、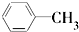 +Cl2 +Cl2
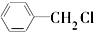 +HCl +HCl | |||
B、2CH3CH2OH+O2
| |||
C、ClCH2CH=CH2+NaOH
| |||
D、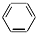 +HONO2 +HONO2
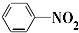 +H2O +H2O |
一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g),达到平衡后测得A气体的浓度为2.5mol/L,当恒温下将密闭容器的容积缩小到原体积
时,再达到平衡后,测得A浓度为4.5mol/L,则下列叙述正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、x+y<z |
| C、C的体积分数提高 |
| D、B的转化率降低 |
下列有关离子方程式的书写正确的是( )
| A、铝与氢氧化钠溶液反应:2Al+2OH-+H2O=2AlO2-+2H2↑ |
| B、氯化铁溶液与铁单质反应:Fe3++Fe=2Fe2+ |
| C、钠投入硫酸铜溶液中:2Na+Cu2+═2Na++Cu |
| D、碳酸氢钠溶液中加入烧碱溶液:HCO3-+OH-═CO32-+H2O |
 矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.
矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.