题目内容
5.将仔细打磨过的铝箔,在酒精灯上加热至熔化,轻轻晃动,看到的现象是( )| A. | 熔化的铝滴落 | |
| B. | 熔化的铝开始剧烈燃烧 | |
| C. | 熔化的铝不滴落,好像有一层膜兜着 | |
| D. | 熔化的铝火星四溅 |
分析 将铝箔在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,又因氧化铝的熔点高于铝的熔点,而氧化铝覆盖在铝的表面,所以加热铝箔的时候铝熔化了但是不会滴落;
解答 解:将铝箔在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,形成氧化膜,三氧化二铝的熔点高于铝的熔点,包住了熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落,好像有一层膜兜着,铝在空气中加热不能燃烧,故选C.
点评 本题考查了铝及其氧化物性质的发信息,注意氧化铝高熔点的性质分析,题目较简单.

练习册系列答案
相关题目
15.“长征二号”的动力来源为反应:C2H8N2(偏二甲肼)+2N2O4═2CO2↑+3N2↑+4H2O↑,其中偏二甲肼中N的化合价为-3价,则2molN2O4中被偏二甲肼中碳原子所还原的N2O4物质的量是( )
| A. | 0.75mol | B. | 1.25mol | C. | 1.5mol | D. | 2mol |
16.下列元素中非金属性最强的是( )
| A. | Mg | B. | Na | C. | F | D. | Cl |
13.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 在0.1 mol•L-1NaHCO3溶液中:c(Na+)>c(OH-)>c(HCO3-)>c(H+)>c(CO32-) | |
| B. | 在0.1 mol•L-1Na2CO3溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 一定量(NH4)2SO4与NH3•H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) | |
| D. | 向0.4 mol/L CH3COOK溶液中加入等体积1.2 mol/L HCl溶液:c(CH3COO-)+c(CH3COOH)=0.4 mol/L |
20.下列实验操作中错误的是( )
| A. | 分液中,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 称量氢氧化钠固体时,将氢氧化钠固体放在垫有滤纸的托盘 | |
| C. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| D. | 称量时,砝码应放在托盘天平的右盘 |
17.下列事实不属于盐类水解应用的是( )
| A. | 明矾、氯化铁晶体常用于净水或消毒 | |
| B. | 实验室通常使用热的纯碱溶液去除油污 | |
| C. | 实验室配制FeCl3溶液时加入少量稀盐酸 | |
| D. | 加热稀醋酸溶液其pH稍有减少 |
14.利用如图所示装置模拟电解原理在工业生产上的应用,下列说法正确的是( )
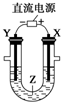

| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的Cu2+浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 制取金属镁时,Z是熔融的氯化镁 |
15.下列溶液或浊液中,关于离子浓度的说法正确的是( )
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-)<c(HCO3-),且3c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| C. | 0.2 mol•L-1的醋酸(CH3COOH)溶液与0.1 mol•L-1NaOH溶液等体积混合后:c(CH3COO-)+2 c(OH-)=c(CH3COOH)+2c(H+) | |
| D. | 常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4悬浊液中的c(Ag+)一定小于AgCl悬浊液中的c(Ag+) |