题目内容
20.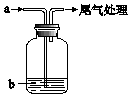 将气体a通入溶液b中,始终无明显变化的是( )
将气体a通入溶液b中,始终无明显变化的是( )| 气体a | 溶液b | |
| A | Cl2 | NaBr |
| B | CO2 | CaCl2 |
| C | SO2 | Ba(NO3)2 |
| D | NO2 | FeSO4 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯气与NaBr反应生成溴;
B.二氧化碳与氯化钙不反应;
C.二氧化硫与硝酸钡发生氧化还原反应;
D.NO2与硫酸亚铁发生氧化还原反应.
解答 解:A.氯气与NaBr反应生成溴,溶液b为颜色由无色变为橙色,故A不选;
B.二氧化碳与氯化钙不反应,无明显变化,故B选;
C.二氧化硫与硝酸钡发生氧化还原反应,生成白色沉淀,故C不选;
D.NO2与硫酸亚铁发生氧化还原反应,溶液由浅绿色变为黄色,故D不选;
故选B.
点评 本题考查化学实验的评价,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
10.下列说法正确的是( )
| A. | 用于纺织的棉花和蚕丝的主要成分是纤维素 | |
| B. | 75%的乙醇溶液可用于医疗消毒,福尔马林可用于浸制动物标本,二者所含原理一样 | |
| C. | 食物中的淀粉类物质,通过人体中酶的催化作用下转化为酒精 | |
| D. | 向鸡蛋清的溶液中加入浓硫酸铜溶液,可观察到蛋白质发生凝聚,再加入蒸馏水,振荡后蛋白质又发生溶解 |
11.下列递变规律正确的是( )
| A. | 酸性HF>HCl>HBr>HI | B. | 热稳定性HI>HRr>HCl>HF | ||
| C. | 非金属性F>Cl>Br>I | D. | 原子半径F>Cl>Br>I |
15.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 醋酸的电离程度增大,c(H+)亦增大 | |
| C. | 再加入10 mL pH=11 NaOH溶液,混合液pH=7 | |
| D. | 溶液中$\frac{{c[CH}_{3}{COO}^{-}]}{{c[CH}_{3}COOH]{c[OH}^{-}]}$不变 |
5.根据图的转化关系判断,下列说法正确的是(反应条件已略去)( )
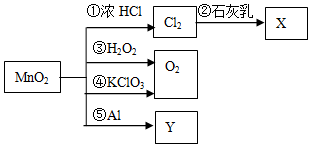

| A. | 反应①中氧化剂与还原剂的物质的量之比为1:4 | |
| B. | 利用反应②可制漂白粉,反应⑤可制金属Mn | |
| C. | 生成等质量的O2,反应③和④转移的电子数相等 | |
| D. | 在反应①③④⑤中,MnO2均作氧化剂 |
12.室温下,向100mL 0.1mol/L NH4Cl溶液中加入下列物质.有关结论正确的是( )
| 加入的物质 | 结论 | |
| A. | 100 mL 0.1 mol/L盐酸 | 溶液中2c=c(Cl-) |
| B. | 0.01 mol Na2O2固体 | 反应完全后,溶液pH增大,c(Na+)=2c(Cl-) |
| C. | 100 mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| D. | 100 mL 0.1 mol/L NH3•H2O | 溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$减小 |
| A. | A | B. | B | C. | C | D. | D |
9.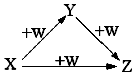 X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )
X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )
①Na、Na2O、Na2 O2 ②AlCl3、Al(OH)3、NaAlO2
③Fe、FeCl2、FeCl3 ④NaOH、Na2CO3、NaHCO3.
 X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )
X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )①Na、Na2O、Na2 O2 ②AlCl3、Al(OH)3、NaAlO2
③Fe、FeCl2、FeCl3 ④NaOH、Na2CO3、NaHCO3.
| A. | ①②④ | B. | ②④ | C. | ①②③ | D. | ①②③④ |
10.下列有关Na2CO3和NaHCO3比较中,不正确的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 相同温度下,0.1mol•L-1盐溶液的pH值:Na2CO3>NaHCO3 | |
| C. | 等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应放出气体的量:Na2CO3<NaHCO3 | |
| D. | 相同温度下,0.1mol•L-1盐溶液分别与0.1mol•L-1HCl反应的剧烈程度:Na2CO3>NaHCO3 |