题目内容
下列有关说法不正确的是( )
| A、相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
| B、0.1 mol Fe与足量盐酸反应,转移的电子数为0.3NA(NA为阿伏加德罗常数的值) |
| C、标准状况下,0.3mol二氧化硫中含有氧原子数为0.6NA |
| D、常温常压下,足量的Fe在1 mol Cl2中充分燃烧,转移的电子数为2NA |
考点:阿伏加德罗常数,氧化性、还原性强弱的比较
专题:
分析:A.离子的氧化性是:Fe3+>Cu2+>Zn2+;
B.Fe与足量盐酸反应反应生成二价铁离子;
C.依据二氧化硫分子式结合物质的量计算氧原子数;
D.铁与氯气反应生成氯化铁,铁足量,需要根据氯气的量计算转移的电子数.
B.Fe与足量盐酸反应反应生成二价铁离子;
C.依据二氧化硫分子式结合物质的量计算氧原子数;
D.铁与氯气反应生成氯化铁,铁足量,需要根据氯气的量计算转移的电子数.
解答:
解:A.根据金属活动性顺序可知金属性由强到弱:Zn>Fe>Cu,而离子的氧化性却是:Fe3+>Cu2+>Zn2+,故A正确;
B.Fe与足量盐酸反应反应生成二价铁离子,转移的电子数为0.2NA,故B错误;
C.依据二氧化硫分子式结合物质的量计算氧原子数,0.3mol二氧化硫中含有氧原子数=0.3mol×2×NA=0.6NA,故C正确;
D.1mol氯气与足量的铁反应最多得到2mol电子,转移的电子数为2NA,故D正确.
故选B.
B.Fe与足量盐酸反应反应生成二价铁离子,转移的电子数为0.2NA,故B错误;
C.依据二氧化硫分子式结合物质的量计算氧原子数,0.3mol二氧化硫中含有氧原子数=0.3mol×2×NA=0.6NA,故C正确;
D.1mol氯气与足量的铁反应最多得到2mol电子,转移的电子数为2NA,故D正确.
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
在 分子中,处于同一平面上的原子数最多可能有( )
分子中,处于同一平面上的原子数最多可能有( )
 分子中,处于同一平面上的原子数最多可能有( )
分子中,处于同一平面上的原子数最多可能有( )| A、12个 | B、14个 |
| C、18个 | D、20个 |
在核电荷数为1~18的原子中,原子的最外层电子数等于次外层电子数的有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为1.00g/L,则混合气体中N2和CH4的体积之比为( )
| A、8:7 | B、1:4 |
| C、4:1 | D、1:1 |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、在标准状况下,体积为22.4L的物质都是1mol |
| B、在非标状况下,1mol任何气体的体积不可能是22.4L |
| C、在标准状况下,1mol H2O和1mol H2的体积都为22.4L |
| D、同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同 |
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
| A、1L 1mol?L-1的CH3COOH溶液中含有NA个氢离子 | ||
| B、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol?L-1 | ||
| C、在1L 0.1 mol?L-1CuSO4溶液中,阴离子总数大于0.1 NA | ||
D、VLCO和NO的混合气体中含有的氧原子个数为
|
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,18克H2O所含电子数为10 NA |
| B、将1mol FeCl3全部化成胶体,其中氢氧化铁胶粒数为NA |
| C、在常温常压下,11.2L氧气所含的原子数目为NA |
| D、标准状况下2.24L的SO3所含的原子数为0.4NA |
下列化学用语中,不正确的是( )
A、氯原子结构示意图: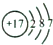 |
B、HCl的电子式: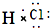 |
| C、乙烯的结构简式:CH2=CH2 |
D、乙炔的比例模型: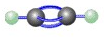 |
能用分液漏斗分离的混合物是( )
| A、液溴和四氯化碳 |
| B、乙醇和乙酸 |
| C、生石灰和乙醇溶液 |
| D、苯和蒸馏水 |