题目内容
13.甲、乙、丙、丁四种易溶于水的物质分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成.已知:①向甲溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成;
②丙将溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;
③1mol/L丁溶液中c(H+)=2mol/L.
下列结论不正确的是( )
| A. | 甲溶液含有Cl- | B. | 乙溶液含有Mg2+ | C. | 丙溶液含有Ba2+ | D. | 丁溶液含有SO42- |
分析 向甲溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,说明甲中含有Cl-;将丙溶液分别与其他三种物质的溶液混合,可以形成白色沉淀的只有BaSO4、BaCO3、Mg(OH)2,因此丙只能是Ba(OH)2,1mol/L丁溶液中c(H+)=2mol/L,说明丁是硫酸;根据离子间的共存可知甲为MgCl2,乙是NH4HCO3 .
解答 解:①向甲溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,说明甲中含有Cl-;②将丙溶液分别与其他三种物质的溶液混合,可以形成白色沉淀的只有BaSO4、BaCO3、Mg(OH)2,因此丙只能是Ba(OH)2,③1mol/L丁溶液中c(H+)=2mol/L,说明丁是硫酸;根据离子间的共存可知甲为MgCl2,乙是NH4HCO3 则可推出甲是MgCl2,乙是NH4HCO3,丙是Ba(OH)2,丁是H2SO4,B错误,故选B.
点评 本题为推断题,做题时注意题中的反应现象,找出突破口,抓住物质的性质是关键,题目难度中等.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
3.元素的性质随原子序数的递增呈周期性变化的原因是( )
| A. | 元素原子的电子层数呈周期性变化 | |
| B. | 元素原子的核外电子排布呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素原子半径呈周期性变化 |
4.要证明某溶液中不含有Fe3+,而可能含有Fe2+,合理顺序是( )
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
| A. | ①③② | B. | ①②③ | C. | ②③① | D. | ②①③ |
1.下列过程有热量放出的是( )
| A. | 水变成水蒸气 | B. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 | ||
| C. | 焦炭与二氧化碳气体发生的反应 | D. | Na与H2O反应 |
18.下表是周期表中的一部分,根据①-⑩在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F、O,还原性最强的单质是Na,可用于制半导体材料的元素是Si;
(2)最高价氧化物的水化物酸性最强的是HClO4,呈两性的是Al(OH)3,最高价氧化物的水化物碱性最强的是NaOH,电子式为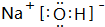 ;
;
(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是Na;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是PH3;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加缓慢(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式Be+2HCl═BeCl2+H2↑.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑦ | ⑧ | ⑩ | ||||
| 3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(2)最高价氧化物的水化物酸性最强的是HClO4,呈两性的是Al(OH)3,最高价氧化物的水化物碱性最强的是NaOH,电子式为
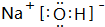 ;
;(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是Na;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是PH3;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加缓慢(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式Be+2HCl═BeCl2+H2↑.
3.最近,科学家冶炼了纯度高达99.999%的铁,你估计它不会具有的性质是( )
| A. | 硬度比生铁低 | B. | 在潮湿空气中放置不易生锈 | ||
| C. | 可溶在稀H2S04中 | D. | 熔点比生铁低 |
 现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
现欲用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答: