题目内容
写出下列反应的离子方程式
①碳酸氢钠溶液与少量石灰水反应
②碳酸氢钠溶液与过量石灰水反应
③等物质的量氢氧化钡溶液与碳酸氢铵溶液混合
④向溴化亚铁溶液通入足量的氯气
⑤向溴化亚铁溶液通入少量氯气
⑥向碘化亚铁溶液通入足量氯气
⑦向碘化亚铁溶液通入少量氯气
⑧苯酚钠与醋酸溶液
⑨苯酚钠溶液中通入少量CO2
⑩硝酸银溶液中滴加氨水至过量 .
①碳酸氢钠溶液与少量石灰水反应
②碳酸氢钠溶液与过量石灰水反应
③等物质的量氢氧化钡溶液与碳酸氢铵溶液混合
④向溴化亚铁溶液通入足量的氯气
⑤向溴化亚铁溶液通入少量氯气
⑥向碘化亚铁溶液通入足量氯气
⑦向碘化亚铁溶液通入少量氯气
⑧苯酚钠与醋酸溶液
⑨苯酚钠溶液中通入少量CO2
⑩硝酸银溶液中滴加氨水至过量
考点:离子方程式的书写
专题:离子反应专题
分析:①石灰水完全反应,生成碳酸钙、碳酸钠和水;
②碳酸氢钠完全反应,生成碳酸钙、NaOH和水;
③等物质的量反应,生成硫酸钡、水、一水合氨;
④亚铁离子、溴离子均全部被氧化;
⑤少量氯气,只有亚铁离子被氧化;
⑥亚铁离子、碘离子均全部被氧化;
⑦少量氯气,只有碘离子被氧化;
⑧反应生成苯酚和醋酸钠;
⑨反应生成苯酚和碳酸氢钠;
⑩滴加氨水至过量,得到银氨溶液.
②碳酸氢钠完全反应,生成碳酸钙、NaOH和水;
③等物质的量反应,生成硫酸钡、水、一水合氨;
④亚铁离子、溴离子均全部被氧化;
⑤少量氯气,只有亚铁离子被氧化;
⑥亚铁离子、碘离子均全部被氧化;
⑦少量氯气,只有碘离子被氧化;
⑧反应生成苯酚和醋酸钠;
⑨反应生成苯酚和碳酸氢钠;
⑩滴加氨水至过量,得到银氨溶液.
解答:
解:①石灰水完全反应,生成碳酸钙、碳酸钠和水,离子反应为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故答案为:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O;
②碳酸氢钠完全反应,生成碳酸钙、NaOH和水,离子反应为HCO3-+OH-+Ca2+=CaCO3↓+H2O,故答案为:HCO3-+OH-+Ca2+=CaCO3↓+H2O;
③等物质的量反应,生成硫酸钡、水、一水合氨,离子反应为Ba2++2OH-+NH4++HCO3-=BaCO3↓+H2O+NH3?H2O,
故答案为:Ba2++2OH-+NH4++HCO3-=BaCO3↓+H2O+NH3?H2O;
④亚铁离子、溴离子均全部被氧化,离子反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故答案为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-;
⑤少量氯气,只有亚铁离子被氧化,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
⑥亚铁离子、碘离子均全部被氧化,离子反应为2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-,故答案为:2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-;
⑦少量氯气,只有碘离子被氧化,离子反应为2I-+Cl2=I2+2Cl-,故答案为:2I-+Cl2=I2+2Cl-;
⑧反应生成苯酚和醋酸钠,离子反应为C6H5O-+CH3COOH=C6H5OH+CH3COO-,故答案为:C6H5O-+CH3COOH=C6H5OH+CH3COO-;
⑨反应生成苯酚和碳酸氢钠,离子反应为C6H5O-+H2O+CO2=C6H5OH+HCO3-,故答案为:C6H5O-+H2O+CO2=C6H5OH+HCO3-;
⑩滴加氨水至过量,得到银氨溶液,离子反应为Ag++2NH3?H2O=Ag(NH3)2++2H2O,故答案为:Ag++2NH3?H2O=Ag(NH3)2++2H2O.
②碳酸氢钠完全反应,生成碳酸钙、NaOH和水,离子反应为HCO3-+OH-+Ca2+=CaCO3↓+H2O,故答案为:HCO3-+OH-+Ca2+=CaCO3↓+H2O;
③等物质的量反应,生成硫酸钡、水、一水合氨,离子反应为Ba2++2OH-+NH4++HCO3-=BaCO3↓+H2O+NH3?H2O,
故答案为:Ba2++2OH-+NH4++HCO3-=BaCO3↓+H2O+NH3?H2O;
④亚铁离子、溴离子均全部被氧化,离子反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故答案为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-;
⑤少量氯气,只有亚铁离子被氧化,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
⑥亚铁离子、碘离子均全部被氧化,离子反应为2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-,故答案为:2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-;
⑦少量氯气,只有碘离子被氧化,离子反应为2I-+Cl2=I2+2Cl-,故答案为:2I-+Cl2=I2+2Cl-;
⑧反应生成苯酚和醋酸钠,离子反应为C6H5O-+CH3COOH=C6H5OH+CH3COO-,故答案为:C6H5O-+CH3COOH=C6H5OH+CH3COO-;
⑨反应生成苯酚和碳酸氢钠,离子反应为C6H5O-+H2O+CO2=C6H5OH+HCO3-,故答案为:C6H5O-+H2O+CO2=C6H5OH+HCO3-;
⑩滴加氨水至过量,得到银氨溶液,离子反应为Ag++2NH3?H2O=Ag(NH3)2++2H2O,故答案为:Ag++2NH3?H2O=Ag(NH3)2++2H2O.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应及氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
某混合气体G可能含有CO、CO2、SO2、H2O等气体,用a.无水CuSO4、b.澄清石灰水、c.灼热CuO、d.碱石灰、e.酸性品红溶液、f.定量酸性高锰酸钾溶液等药品可将其一一检出,检出的正确顺序是( )
| A、G→a→e→b→f→d→c |
| B、G→c→d→b→e→f→a |
| C、G→a→e→f→b→d→c |
| D、G→b→e→f→a→d→c |
下列反应处于平衡状态,2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,欲提高平衡常数K的值,应采取的措施是( )
| A、降低温度 | B、增大压力 |
| C、加入氧气 | D、去掉三氧化硫 |
化学家从反应C2H6(g)+Cl2(g)→C2H5Cl(l)+HCl(g)中受到启发,提出在农药和有机合成工业中可获得副产品盐酸,这一设想已成为现实.试指出从上述反应体系中得到盐酸可采用的分离方法是( )
| A、蒸馏法 | B、水洗法 |
| C、分液法 | D、过滤法 |
下列各组溶液,均含有等物质的量的溶质,如将3种溶液完全混合后,不会产生沉淀的是( )
| A、NaAlO2、NH4Cl、HCl |
| B、FeCl3、KSCN、HCl |
| C、CaCl2、NaHCO3、NaOH |
| D、AlCl3、Ba(OH)2、HNO3 |
 2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest).有一类硼烷也好似鸟巢,故称为巢式硼烷.巢式硼烷除B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化.如图是三种巢式硼烷,有关说法正确的是( )
2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest).有一类硼烷也好似鸟巢,故称为巢式硼烷.巢式硼烷除B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化.如图是三种巢式硼烷,有关说法正确的是( )| A、这类巢式硼烷的通式是BnHn+4 | ||||
B、2B5H9+12O2
| ||||
| C、8个硼原子的巢式硼烷化学式应为B8H10 | ||||
| D、硼烷与水反应是非氧化还原反应 |
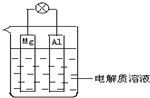 如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):