题目内容
0.5molNH3中含 个NH3分子,质量为 ,H原子 mol,质子 mol,在标准状况下的体积为 ,将此气体溶于水配成配成100ml溶液,则此溶液物质的量浓度是 .
考点:物质的量的相关计算
专题:计算题
分析:根据N=nNA计算NH3分子数目,根据m=nM计算NH3质量,结合分子含有H原子数目计算H原子物质的量,每个NH3分子含有10个质子,故质子物质的量为NH3分子的10倍,根据V=nVm计算NH3体积,根据c=
计算氨水溶液的物质的量浓度.
| n |
| V |
解答:
解:0.5molNH3中含有分子数目=0.5mol×6.02×1023mol-1=3.01×1023,其质量为0.5mol×17g/mol=8.5g,含有H原子物质的量=0.5mol×3=1.5mol,含有质子物质的量=0.5mol×10=5mol,在标准状况下,占有的体积为0.5mol×22.4L/mol=11.2L,将此气体溶于水配成配成100ml溶液,则此溶液物质的量浓度是
=5mol/L,
故答案为:3.01×1023;8.5g;1.5;5;11.2 L;5 mol/L.
| 0.5mol |
| 0.1L |
故答案为:3.01×1023;8.5g;1.5;5;11.2 L;5 mol/L.
点评:本题考查物质的量有关计算,比较基础,注意对公式的理解,侧重对基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于电解质溶液的叙述正确的是( )
| A、常温下,由0.1mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH?B++OH- |
| B、常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
下列物质中属于碱性氧化物的是( )
| A、O2 |
| B、Na2O |
| C、NaClO |
| D、SO2 |
下列反应的离子方程式正确的是( )
| A、稀硫酸与氢氧化钡溶液反应:SO42-+2H++2OH-+Ba2+═BaSO4↓+2H2O |
| B、饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
| C、氧化铜与稀硫酸反应:2H++O2-═H2O |
| D、澄清石灰水与氯化铜溶液反应:Cu2++Ca(OH)2═Cu(OH)2↓+Ca2+ |
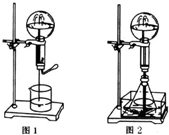 喷泉是一种常见的自然现象,其产生原因是存在压强差.
喷泉是一种常见的自然现象,其产生原因是存在压强差.