题目内容
17.下列物质属于弱电解质的是( )| A. | CO2 | B. | 氯水 | C. | NH3•H2O | D. | Ba(OH)2 |
分析 在水溶液里或者熔融状态下只能部分电离的电解质是弱电解质,弱电解质包括弱酸、弱碱、水与少数盐,据此解答.
解答 解:A、二氧化碳在水溶液中导电和其本身无关,在熔融状态下不能导电,故为非电解质,不是电解质,故A错误;
B、氯水是氯气的水溶液,是混合物,既不是电解质也不是非电解质,故B错误;
C、一水合氨在水溶液中只能部分电离,故为弱电解质,故C正确;
D、氢氧化钡在水溶液中能完全电离,故为强电解质,故D错误.
故选C.
点评 本题考查了强弱电解质的判断,难度不大,解题关键是明确电解质的强弱是以电离程度判断的,易错项为A,注意二氧化碳的水溶液导电的原因是二氧化碳与水生成碳酸的原因,二氧化碳本身不电离,是非电解质.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
7.下列离子方程式书写不正确的是( )
| A. | 用盐酸除铁锈 Fe2O3+6H+=2Fe3++3H2O | |
| B. | 将Na放入水中 2Na+2H2O=2Na++2OH-+H2↑ | |
| C. | 氢氧化铝溶于盐酸 OH-+H+=H2O | |
| D. | 小苏打与氢氧化钠反应 HCO3-+H+=CO2↑+H2O |
5.下列变化过程中,属于吸热反应的是( )
(1)液氨汽化(2)将胆矾加热变为白色粉末(3)浓硫酸稀释
(4)水的液化(5)酸碱中和生成水(6)氯化铵与氢氧化钡的反应.
(1)液氨汽化(2)将胆矾加热变为白色粉末(3)浓硫酸稀释
(4)水的液化(5)酸碱中和生成水(6)氯化铵与氢氧化钡的反应.
| A. | (2)(6) | B. | (1)(2)(3)(6) | C. | (3) | D. | (2)(4)(6) |
12.下列电离方程式正确的是( )
| A. | NH4Cl?NH4++Cl- | B. | H2S?2H++S2- | ||
| C. | KHCO3?K++H+++CO3- | D. | CH3COONH4=NH4++CH3COO- |
9.下列过程一定释放能量的是( )
| A. | 化合反应 | B. | 分解反应 | ||
| C. | 反应物分子中化学键断裂 | D. | 原子组合成分子 |
6.下列各分子中所有原子都满足最外层为8电子稳定结构的是( )
| A. | BeCl2 | B. | CO2 | C. | HCl | D. | N2 |
7.酸、碱、盐均属于电解质,它们的水溶液中存在各种平衡.
(1)氨水是中学常见碱
①下列事实可证明氨水是弱碱的是BD(填字母序号).
A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
B.常温下,0.1mol•L-1氨水pH为11
C.铵盐受热易分解
D.常温下,0.1mol•L-1氯化铵溶液的pH为5
②下列方法中,可以使氨水电离程度增大的是BC(填字母序号).
A.通入氨气 B.加入少量氯化铁固体
C.加水稀释 D.加入少量氯化铵固体
(2)盐酸和醋酸是中学常见酸
用0.1mol•L-1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol•L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线.
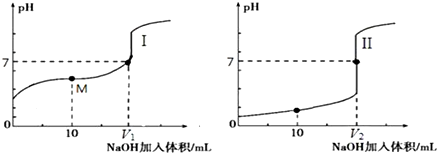
①滴定醋酸的曲线是I(填“I”或“II”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是0.1mol•L-1醋酸溶液.
③V1和V2的关系:V1<V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是c(CH3COO-)>c (Na+)>c (H+)>c (OH-).
(3)为了研究难溶盐的沉淀溶解平衡和沉淀转化,某同学设计如下实验.
已知:ⅠAgSCN是白色沉淀.
Ⅱ相同温度下,Ksp(AgI)=8.3×10?17,Ksp (AgSCN )=1.0×10?12.
①步骤3中现象a是出现白色沉淀.
②用沉淀溶解平衡原理解释步骤4的实验现象AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgSCN>AgI.Ag+与I-反应生成AgI黄色沉淀,AgSCN的溶解平衡正向移动.
③向50mL 0.005mol•L?1的AgNO3溶液中加入150mL0.005mol•L?1的 KSCN溶液,混合后溶液中Ag+的浓度约为4×10?10mol•L?1.(忽略溶液体积变化)
(1)氨水是中学常见碱
①下列事实可证明氨水是弱碱的是BD(填字母序号).
A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
B.常温下,0.1mol•L-1氨水pH为11
C.铵盐受热易分解
D.常温下,0.1mol•L-1氯化铵溶液的pH为5
②下列方法中,可以使氨水电离程度增大的是BC(填字母序号).
A.通入氨气 B.加入少量氯化铁固体
C.加水稀释 D.加入少量氯化铵固体
(2)盐酸和醋酸是中学常见酸
用0.1mol•L-1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol•L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线.

①滴定醋酸的曲线是I(填“I”或“II”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是0.1mol•L-1醋酸溶液.
③V1和V2的关系:V1<V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是c(CH3COO-)>c (Na+)>c (H+)>c (OH-).
(3)为了研究难溶盐的沉淀溶解平衡和沉淀转化,某同学设计如下实验.
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1Fe(NO3)3溶液. | 溶液变为红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴 3mol•L-1AgNO3溶液. | 现象a出现白色沉淀,溶液红色变浅. |
| 步骤4:向步骤1余下的浊液中加入5滴 3mol•L-1KI溶液. | 出现黄色沉淀. |
Ⅱ相同温度下,Ksp(AgI)=8.3×10?17,Ksp (AgSCN )=1.0×10?12.
①步骤3中现象a是出现白色沉淀.
②用沉淀溶解平衡原理解释步骤4的实验现象AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgSCN>AgI.Ag+与I-反应生成AgI黄色沉淀,AgSCN的溶解平衡正向移动.
③向50mL 0.005mol•L?1的AgNO3溶液中加入150mL0.005mol•L?1的 KSCN溶液,混合后溶液中Ag+的浓度约为4×10?10mol•L?1.(忽略溶液体积变化)