题目内容
4.下列离子方程式书写正确的是( )| A. | 醋酸除去水垢中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铜和浓硝酸反应:Cu+4H++2NO${\;}_{3}^{-}$═Cu2++2NO2↑+2H2O | |
| C. | 向氨水中通入过量SO2:2NH3•H2O+SO2═2NH${\;}_{4}^{+}$+SO${\;}_{3}^{2-}$+H2O | |
| D. | H2SO4溶液和Ba(OH)2溶液:H++SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓+H2O |
分析 A.醋酸为弱酸应保留化学式;
B.反应生成硝酸铜和二氧化氮、水;
C.二氧化硫过量反应生成亚硫酸氢铵;
D.原子个数不守恒,电荷数不守恒.
解答 解:A.醋酸除去水垢中,离子方程式:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故A错误;
B.铜和浓硝酸反应,离子方程式:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故B正确;
C.将过量SO2气体通入氨水中,反应生成亚硫酸氢铵,反应的离子方程式为:SO2+NH3•H2O=NH4++HSO3-,故C错误;
D.H2SO4溶液和Ba(OH)2溶液,离子方程式:2H++2OH-+SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓+2H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写判断,明确反应实质及离子方程式书写方法是解题关键,注意反应物用量对反应的影响,注意化学式的拆分,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
14.下列物质的化学式与俗称不相符的是( )
| A. | Na2CO3-苏打 | B. | BaCO3-重金石 | C. | NH4NO3-硝铵 | D. | NaOH-火碱 |
15.下列说法正确的是( )
| A. | 常温下将pH=2的硫酸和pH=12的MOH溶液等体积混合,所得溶液pH≤7 | |
| B. | 已知同温度相同浓度的NaNO2溶液比NaF溶液的碱性强,所以氢氟酸的酸性比亚硝酸的弱 | |
| C. | 常温下,将醋酸钠、盐酸两溶液混合后,溶液呈中性,则有c(Na+)>c(Cl-)=c(CH3COOH) | |
| D. | pH相等的NH4Cl、(NH4)2SO4、NH4HSO4三种溶液物质的量浓度为c(NH4Cl)>c((NH4)2SO4)=c(NH4HSO4) |
12.在下列各溶液中离子一定能大量共存的是( )
| A. | 强碱溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含0.1mol?L-1Fe3+的溶液中:K+、Ba2+、NO3-、SO42- | |
| C. | 含0.1mol?L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 室温下c(H+)=0.1mol?L-1的溶液中:Na+、Fe3+、NO3-、SO42- |
19.下列离子方程式不正确的是( )
| A. | Fe304与稀硝酸反应的离子方程式为:3Fe3O4+28H++N03一═9Fe3++NO↑+14H20 | |
| B. | 用稀硫酸除去铜绿:4H++Cu2(OH)2CO3═2Cu2++C02↑+3H2O | |
| C. | 向NH4Al(S04)2溶液中滴人Ba(OH)2溶液恰好使S042-完全沉淀:2Ba2-+NH4++Al3++2SO42-+40H-═Al(OH)3↓+NH3•H20+2BaSO4↓ | |
| D. | 少量氢氧化钙溶液与碳酸氢钠溶液混合:Ca2++OH-+HC03-═CaCO3↓+H2O |
9.短周期元素甲、乙、丙、丁的原子序数依次增大,甲形成的化合物种类最多,乙、丙、丁为同周期元素,其最高价氧化物对应的水化物两两之间能相互反应,丁的原子序数为甲、乙原子序数之和.下列说法正确的是( )
| A. | 元素丙的单质可用于冶炼金属 | |
| B. | 甲的氢化物比丁的氢化物热稳定性强 | |
| C. | 简单离子半径:乙>丁>丙 | |
| D. | 甲与乙的氧化物均有强氧化性 |
16.铬(Cr)有多种化合物,在工业生产中有广泛的用途.
(1)工业上利用铬铁矿(FeO Cr2O3)冶炼铬的工艺流程如下:
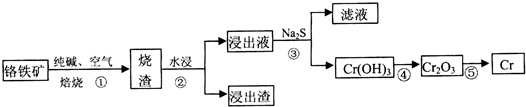 a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
b.浸出液中含有的主要成分为Na2CrO4,向滤液中加酸化的氯化钡溶液有白色沉淀生成,则操作③发生反应的离子方程式CrO42-+Ba2+=BaCrO4↓.
(2)铬的化合物有毒,排放前要经过处理,通常用电解法:
将含Cr2O72-的废水放入电解槽内,加入一定量氯化钠,用铁作电极提供Fe2+,Cr2O72-将Fe2+氧化生成Fe3+,本身被还原生成Cr3+,最后Cr3+和Fe3+以Cr(OH)3和Fe(OH)3的形式除去.铁作电解槽的阳极,阴极反应式为2H++2e-=H2↑,Cr2O72-氧化Fe2+的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
(3)CrO3是一种常见的铬的氧化物,其热稳定性较差,加热时逐步分解.取100gCrO3加热,剩余固体的质量随温度的变化如下表所示.
则x=84.00,y为Cr2O5(写化学式).
(1)工业上利用铬铁矿(FeO Cr2O3)冶炼铬的工艺流程如下:
 a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).b.浸出液中含有的主要成分为Na2CrO4,向滤液中加酸化的氯化钡溶液有白色沉淀生成,则操作③发生反应的离子方程式CrO42-+Ba2+=BaCrO4↓.
(2)铬的化合物有毒,排放前要经过处理,通常用电解法:
将含Cr2O72-的废水放入电解槽内,加入一定量氯化钠,用铁作电极提供Fe2+,Cr2O72-将Fe2+氧化生成Fe3+,本身被还原生成Cr3+,最后Cr3+和Fe3+以Cr(OH)3和Fe(OH)3的形式除去.铁作电解槽的阳极,阴极反应式为2H++2e-=H2↑,Cr2O72-氧化Fe2+的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
(3)CrO3是一种常见的铬的氧化物,其热稳定性较差,加热时逐步分解.取100gCrO3加热,剩余固体的质量随温度的变化如下表所示.
| 温度/K | 480 | 505 | 615 | 730 |
| 质量/g | 94.67 | 92.00 | x | 76.00 |
| 化学式 | Cr3O8 | y | CrO2 | Cr2O3 |
13.有K2SO4、Al2(SO4)3的混合溶液,已知其中的Al3+、SO42-的浓度分别为0.4mol/L、0.7mol/L,则该溶液中K+的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.15mol/L | C. | 0.2mol/L | D. | 0.25mol/L |
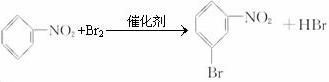 、
、 、
、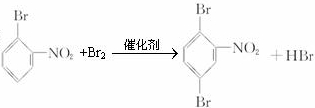 或
或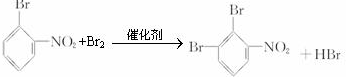 .
.