题目内容
20.锂被誉为“高能金属”.工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在一定条件下反应生成Li2SO4(以及MgSO4、硅铝化合物等物质),进而制备金属锂,其生产流程如下: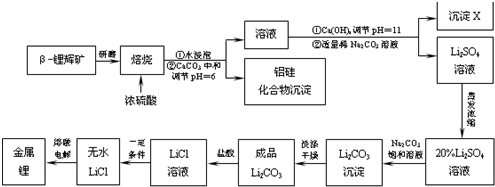
(1)用氧化物形式表示LiAlSi2O6的组成:Li2O•Al2O3•4SiO2.
(2)沉淀X主要成分为CaCO3和Mg(OH)2.
(3)写出盐酸与Li2CO3反应的离子方程式:Li2CO3+2H+=2Li++H2O+CO2↑.
(4)写出电解熔融LiCl时阴极的电极反应式:Li++e-=Li.
(5)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:前者是浓度过大会使部分Li+沉淀;后者是此时浓度大则有利于Li2CO3沉淀的生成.
(6)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体.试写出氢化锂遇水反应的化学方程式LiH+H2O=LiOH+H2↑.
(7)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂.电解时产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解产生Li2O,电解时产生O2.
分析 工业上用硫酸与β-锂辉矿反应,生成不溶于酸的硅化合物和含少量铝、钙、镁离子的硫酸锂溶液,然后加入氢氧化钙和碳酸钠溶液除去滤液中的铝、钙、镁离子,得到较为纯净的硫酸锂,再将溶液中锂离子转化为溶解度较小碳酸锂,加饱和Na2CO3溶液的目的是使Li+转化生成Li2CO3沉淀,通过恰当方法最终得到单质锂.
(1)将硅酸盐写成二氧化硅和其它氧化物形式,照例而行,保证原子总数,化合价不变,按化合价分别写化学式,如有多个原子,在前面加上系数,使之成为倍数;
(2)溶液中含有镁离子;
(3)盐酸与Li2CO3反应生成氯化锂,水和二氧化碳;
(4)电解时阴极得电子;
(5)第一次用碳酸钠是调节pH值,第二次用碳酸钠是为了沉淀Li2CO3;
(6)氢化锂具有还原性,可与水发生氧化还原反应生成氢气;
(7)LiCl溶液加热蒸干,LiCl水解生成的LiOH,受热分解产生Li2O,电解Li2O的熔融物得到氧气.
解答 解:(1)LiAlSi2O6可表示为:Li2O•Al2O3•4SiO2,故答案为:Li2O•Al2O3•4SiO2;
(2)溶液中含有镁离子,氢氧化镁是沉淀,故答案为:Mg(OH)2;
(3)盐酸与Li2CO3反应的离子方程式Li2CO3+2H+=2Li++H2O+CO2↑,故答案为:Li2CO3+2H+=2Li++H2O+CO2↑;
(4)电解时阴极得电子,电极方程式为Li++e-=Li,故答案为:Li++e-=Li;
(5)碳酸钠可与酸反应,第一次用碳酸钠可起到调节pH值的作用,可沉淀氢氧化镁,第二次用碳酸钠时浓度较大,是为了沉淀Li2CO3,
故答案为:浓度过大会使部分Li+ 沉淀;此时浓度大则有利于Li2CO3沉淀的生成;
(6)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体,是氢化锂和水反应生成氢气和氢氧化锂,反应的化学方程式为:LiH+H2O=LiOH+H2↑,故答案为:LiH+H2O=LiOH+H2↑;
(7)LiCl溶液在加热易发生水解生成LiOH和HCl,LiCl溶液加热蒸干,LiCl水解生成LiOH,受热分解产生Li2O,实际上电解的是LiCl和Li2O的熔融混合物,电解时产生O2.
故答案为:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解产生Li2O,电解时产生O2.
点评 本题主要考查物质的制备,为高考常见题型,侧重于学生的分析能力、实验能力的考查,题目涉及物质的分离、电解原理、盐类的水解等,难度难度较大,掌握实验的原理和流程分析是解题的关键.

 阅读快车系列答案
阅读快车系列答案相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
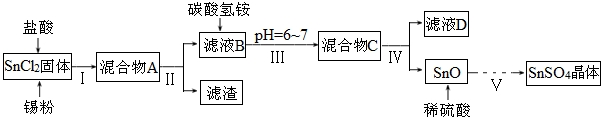
(2)在空气中直接加热CuCl2•2H2O晶体得不到纯的无水CuCl2,原因是2CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(OH)2•CuCl2+2HCl+2H2O(用化学方程式表示).
由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥的HCl气流中加热脱水.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0mol•L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是蓝色褪去,放置一定时间后不恢复原色.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95%.
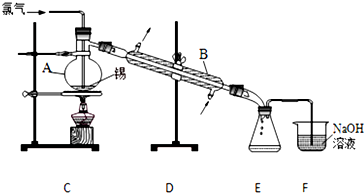
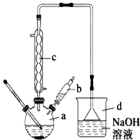 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:步骤1:在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应.
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑.
步骤3:滤液依次用10mL水、8mL 10%的NaOH溶液、10mL 水洗涤,
分液得粗溴苯.
| 苯 | 溴 | 溴苯 | |
| 密度/gcm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
(1)步骤1仪器a中发生的主要反应是
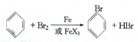 ;
;(2)仪器c的名称是冷凝管,仪器d的作用是吸收HBr防污染,防倒吸;
(3)将b中的液溴慢慢加入到a中,而不能快速加入的原因是防止反应放出的热使C6H6、Br2挥发而影响产率;
(4)仪器c的作用是冷凝回流,回流的主要物质有C6H6、Br2(填化学式);
(5)步骤4得到的粗产品中还含有杂质苯,已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是蒸馏.
(6)实验结束后,试设计实验方案检验d装置所得溶液中含有Br-:
实验操作:取少量d中溶液于试管中,滴加过量稀HNO3,再加入AgNO3溶液;
实验现象和结论:有淡黄色沉淀生成,溶液中含有Br-.
某实验小组拟用酸碱中和滴定法测定食醋的总酸量(CH3COOH,g/100mL).
(一)、实验用品:市售食用白醋样品500mL(商标注明:总酸量:3.5g-5g/100mL)(下称“原醋”),0.1000mol/LNaOH标准溶液,蒸馏水,0.1%甲基橙溶液、0.1%酚酞溶液;仪器自选.
(二)、实验原理:化学方程式CH3COOH+NaOH=CH3COONa+H2O
(三)、实验步骤:
(1)配制待测食醋溶液
准确量取10.00mL原醋,配制成100.00mL待测食醋溶液(下称“待测液”).完成该步骤,需要的一种定量仪器是100ml容量瓶(填仪器名称)
(2)量取一定体积的待测液
用酸式滴定管取20.00mL待测液于锥形瓶中.加1-2滴0.1%酚酞溶液做指示剂
(3)盛装标准NaOH溶液,记录为NaOH标准溶液体积的初读数.
(4)滴定操作:滴定时一手控制滴定管,一手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色变化直到滴定终点.判断滴定终点的现象是由无色变为浅红色,半分钟内不褪色.
记录NaOH的终读数.重复滴定4次.
(四)、实验记录及数据处理(请完成相关填空)
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(待测液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.95 | 15.20 | 15.15 | 16.95 |
| V(NaOH)/mL(消耗) | 14.95 | 15.00 | 15.05 | 16.95 |
(6)消耗NaOH溶液的平均值是15.00mL.
(7)待测液的浓度是0.075mol/L.
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 0.5molO3与11.2LO2所含的分子数一定相等 | |
| C. | 物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-数为NA | |
| D. | 1molFe与足量稀盐酸反应时,转移电子的数目为3NA |
 .
. .
.
 某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值.该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值.该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定: