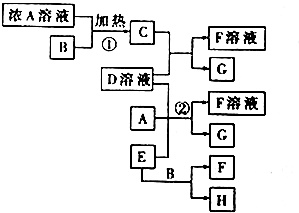
题目内容
4.下列实验的反应原理用离子方程式表示正确的是( )| A. | 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3•H2O+H3O+ | |
| B. | 将16.8g铁粉投入100mL4.0mol/L的HNO3溶液中(还原产物只有NO):6Fe+20H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O | |
| C. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O | |
| D. | 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
分析 A.水解为可逆反应;
B.Fe的物质的量为$\frac{16.8g}{56g/mol}$=0.3mol,硝酸的物质的量为0.1L×4.0mol/L=0.4mol,物质的量比为3:4,硝酸不足;
C.草酸在离子反应中保留化学式;
D.Al与NaOH溶液反应生成偏铝酸钠和氢气,而Mg不反应.
解答 解:A.室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱的离子反应为NH4++2H2O?NH3•H2O+H3O+,故A错误;
B.Fe的物质的量为$\frac{16.8g}{56g/mol}$=0.3mol,硝酸的物质的量为0.1L×4.0mol/L=0.4mol,硝酸不足,离子反应为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故B错误;
C.用高锰酸钾标准溶液滴定草酸的离子反应为2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O,故C错误;
D.用氢氧化钠溶液除去镁粉中的杂质铝的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
15.有关离子交换法软化硬水的下列叙述中,正确的是( )
| A. | 磺化煤能使具有永久硬度的水软化,因为它能除去水中的Ca2+、Mg2+、SO42-和Cl-等 | |
| B. | 经磺化煤软化处理后,软水中Na+浓度增大 | |
| C. | 磺化煤使硬水软化以及磺化煤的再生,这两种操作可以在同一离子交换柱中同时进行 | |
| D. | 失去软化硬水能力的磺化煤,不可能恢复它的软化能力 |
12.设NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A. | 5.6 g Fe和足量的氯气完全反应失去电子数为0.3NA | |
| B. | 0.1molNa2O2固体与足量的H2O充分反应,转移0.2NA个电子 | |
| C. | 常温常压下,23 g NO2和N2O4的混合气体一定含有NA个氧原子 | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
9.将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判断合理的是( )
| A. | Fe(NO3)x中的x为2 | |
| B. | 稀HNO3在反应中只表现氧化性 | |
| C. | 反应中每还原0.4 mol氧化剂,就有1.2 mol电子被转移 | |
| D. | 磁性氧化铁中的铁元素全部被氧化 |
16.向体积为2L的容器中加入1molN2和6molH2,合成氨.2分钟之后达到平衡,测得氮气为0.6mol.氢气的反应速率是( )
| A. | 0.1 mol•L-1•min-1 | B. | 0.2 mol•L-1•min-1 | ||
| C. | 0.3 mol•L-1•min-1 | D. | 0.6 mol•L-1•min-1 |
13.元素周期表中铋元素的数据如图,下列说法正确的是( )
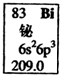

| A. | Bi元素的质量数是209 | |
| B. | Bi原子最外层有5个能量相同的电子 | |
| C. | Bi原子6p亚层有一个未成对电子 | |
| D. | Bi元素的相对原子质量是209.0 |
14.下列说法错误的是( )
| A. | 工业上电解熔融状态的Al2O3制备Al涉及氧化还原反应 | |
| B. | 四川灾区重建使用了大量钢材,钢材是合金 | |
| C. | 金属材料都是导体,非金属材料都是绝缘体 | |
| D. | 合金材料中可能含有非金属元素 |