题目内容
 大理石与盐酸反应的反应速率如图所示,已知反应为放热反应.
大理石与盐酸反应的反应速率如图所示,已知反应为放热反应.(1)写出该反应的离子反应方程式:
(2)反应开始时反应速率加快的原因是
(3)反应后期反应速率下降的原因是
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:发生大理石与氢离子的反应,反应为放热反应,由图可知,开始反应速率增大与温度有关,后来反应速率减小与氢离子浓度有关,以此来解答.
解答:
解:(1)发生大理石与氢离子的反应,离子反应为CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(2)反应开始时反应速率加快的原因是温度升高,反应速率加快,故答案为:温度升高,反应速率加快;
(3)反应后期反应速率下降的原因是反应物浓度减小,反应速率减慢,故答案为:反应物浓度减小,反应速率减慢.
(2)反应开始时反应速率加快的原因是温度升高,反应速率加快,故答案为:温度升高,反应速率加快;
(3)反应后期反应速率下降的原因是反应物浓度减小,反应速率减慢,故答案为:反应物浓度减小,反应速率减慢.
点评:本题考查影响化学反应速率的因素,为高频考点,把握温度、浓度对反应速率的影响为解答的关键,侧重分析能力及应用能力的考查,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
能正确表示下列反应的离子方程式是( )
A、过量的SO2通入氨水中:NH3?H20+SO2
| ||||
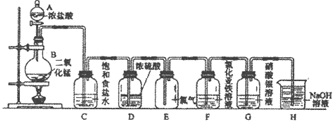
B、实验室制备氯气:MnO2+4H++2Cl-
| ||||
C、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-
| ||||
D、明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-
|
下列因果关系叙述正确的是( )
| A、SO2具有漂白性,故可使酸性KMnO4溶液褪色 |
| B、浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| C、Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg |
| D、Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中Fe也显+3价 |