题目内容
把1.92g铜投入盛有一定量浓硝酸的试管中,金属铜恰好完全溶解,收集到标准状况下NO和NO2混合气体1120mL,求:
(1)产生NO和NO2各自的体积.
(2)参加反应的硝酸的物质的量.
(1)产生NO和NO2各自的体积.
(2)参加反应的硝酸的物质的量.
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:(1)根据n=
计算混合气体的物质的量,令混合气体中NO和NO2物质的量分别为xmol、ymol,利用电子转移守恒、二者物质的量之和列方程,据此计算x、y的值,再根据v=nVm计算NO和NO2各自的体积;
(2)涉及反应有Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,
根据N原子守恒计算,反应的n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2).
| V |
| Vm |
(2)涉及反应有Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,
根据N原子守恒计算,反应的n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2).
解答:
解:n(Cu)=
=0.03mol,n(NO)+n(NO2)=
=0.05mol,
(1)1120mL混合气体的物质的量为0.05mol,令混合气体中NO和NO2物质的量分别为xmol、ymol,
由电子转移守恒有:3x+y=0.03×2,
由二者物质的量之和:x+y=0.05,
联立方程,解得x=0.005,y=0.045,
故NO的体积为0.005mol×22.4L/mol=0.112L,
NO2的体积为0.045mol×22.4L/mol=1.008L,
答:产生NO和NO2各自的体积分别为0.112L、1.008L.
(2)涉及反应有Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,
由方程式可知反应消耗的n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2).
则n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2)=0.03mol×2+0.05mol=0.11mol.
答:参加反应的硝酸的物质的量为0.11mol.
| 1.92g |
| 64g/mol |
| 1.12L |
| 22.4L/mol |
(1)1120mL混合气体的物质的量为0.05mol,令混合气体中NO和NO2物质的量分别为xmol、ymol,
由电子转移守恒有:3x+y=0.03×2,
由二者物质的量之和:x+y=0.05,
联立方程,解得x=0.005,y=0.045,
故NO的体积为0.005mol×22.4L/mol=0.112L,
NO2的体积为0.045mol×22.4L/mol=1.008L,
答:产生NO和NO2各自的体积分别为0.112L、1.008L.
(2)涉及反应有Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,
由方程式可知反应消耗的n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2).
则n(HNO3)=2n(Cu(NO3)2)+n(NO)+n(NO2)=0.03mol×2+0.05mol=0.11mol.
答:参加反应的硝酸的物质的量为0.11mol.
点评:本题考查化学方程式的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意从守恒的角度解答该题,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
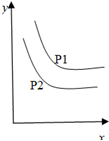 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )| A、上述反应是放热反应 |
| B、a=b |
| C、a>b |
| D、上述反应是吸热反应 |
下列离子方程式正确的是( )
| A、锌粉与稀硝酸反应:Zn+2H+═Zn2++H2↑ | ||||
B、硫酸铵中NH4+的检验:NH4++OH-
| ||||
| C、NH4Al(SO4)2溶液与足量Ba(OH)2溶液混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
D、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
|
下列离子方程式正确的是( )
| A、醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2A(OH)3↓+CO32- |
| C、将过量二氧化硫气体入冷氨水中:SO2+NH3?H2O=HSO3-+NH4+ |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH- |
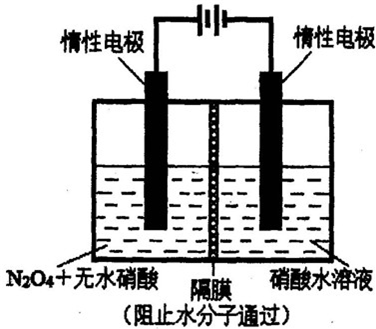 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
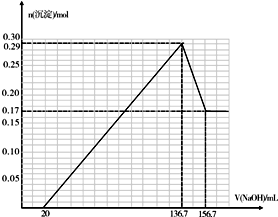
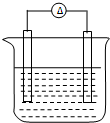 铁片和铜片浸入200mL CuSO4溶液中组成如图所示原电池,若开始时该电池中两电极的总质量为60克,工作一段时间后,硫酸铜恰好反应完.取出铁片和铜片,洗净干燥后称重,总质量为61.6克,试计算:(不考虑铁片直接和硫酸铜的反应)
铁片和铜片浸入200mL CuSO4溶液中组成如图所示原电池,若开始时该电池中两电极的总质量为60克,工作一段时间后,硫酸铜恰好反应完.取出铁片和铜片,洗净干燥后称重,总质量为61.6克,试计算:(不考虑铁片直接和硫酸铜的反应)