题目内容
下列对应化学反应的离子方程式正确的是( )
A、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、KHSO3的水解:HSO3-+H2O?SO32-+H3O+ | ||||
| C、Na2O2与水反应:2Na2O2+2H2O═4Na++4OH-+O2↑ | ||||
| D、少量Ca(HCO3)2溶液与足量的NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.盐酸是强电解质;
B.HSO3-水解生成氢氧根;
C.过氧化物用化学式表示;
D.Ca(HCO3)2溶液和NaOH溶液1:2反应.
B.HSO3-水解生成氢氧根;
C.过氧化物用化学式表示;
D.Ca(HCO3)2溶液和NaOH溶液1:2反应.
解答:
解:A.实验室用浓盐酸与MnO2反应制Cl2:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故A错误;
B.KHSO3的水解:HSO3-+H2O?H2SO3+OH-,故B错误;
C.Na2O2能和水发生反应:2Na2O2+2H2O═4Na++4OH-+O2↑,故C正确;
D.少量Ca(HCO3)2溶液与足量的NaOH溶液反应:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故D错误.
故选C.
| ||
B.KHSO3的水解:HSO3-+H2O?H2SO3+OH-,故B错误;
C.Na2O2能和水发生反应:2Na2O2+2H2O═4Na++4OH-+O2↑,故C正确;
D.少量Ca(HCO3)2溶液与足量的NaOH溶液反应:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故D错误.
故选C.
点评:本题考查离子方程式的书写,题目难度中等,本题中注意把握物质的性质以及反应的过量问题,为易错点.

练习册系列答案
相关题目
向Na2SO3和NaI的物质的量之比为1:1的混合溶液中逐滴滴入氯水,下列离子反应不可能发生的是( )
| A、SO32-+Cl2+H2O→SO42-+2H++2Cl- |
| B、4I-+SO32-+3Cl2+H2O→SO42-+2H++6Cl-+2I2 |
| C、2I-+SO32-+2Cl2+H2O→SO42-+2H++4Cl-+2I2 |
| D、2I-+2SO32-+3Cl2+2H2O→2SO42-+4H++6Cl-+I2 |
下列各组离子能够大量共存的是( )
| A、pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B、使pH试纸显蓝色的溶液中:Cu2+、Fe3+、NO3-、SO42- |
| C、滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32-、NO3- |
| D、水电离出的c(H+)=1×10-13mol?L-1的溶液中:K+、HCO3-、Cl-、NH4+ |
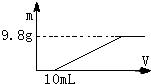 过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )
过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )| A、0.05mol |
| B、0.1mol |
| C、0.2mol |
| D、0.25mol |
 右图是中学化学中一些常见的物质之间发生的一系列转化的框图(反应所需和所产生的水及某些反应条件已略),其中A、B、F、Y为黑色的固体,E、G在常温常压下是气体.
右图是中学化学中一些常见的物质之间发生的一系列转化的框图(反应所需和所产生的水及某些反应条件已略),其中A、B、F、Y为黑色的固体,E、G在常温常压下是气体.


