题目内容
9.需要配制2mol/L的NaCl溶液480mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )| A. | 480mL,56.2g | B. | 500mL,56.2g | C. | 500mL,58.5g | D. | 任意规格,56.2g |
分析 配制2mol/L的NaCl溶液480mL,选择500mL容量瓶,结合m=cVM计算.
解答 解:配制2mol/L的NaCl溶液480mL,选择500mL容量瓶,NaCl的质量为0.5L×2mol/L×58.5g/mol=58.5g,
故选C.
点评 本题考查配制一定浓度的溶液,为高频考点,把握容量瓶的选择、浓度与物质的量的关系为解答的关键,侧重分析与应用能力的考查,注意容量瓶具有固定规格,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
19.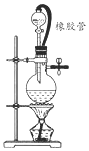 在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管.下列对其作用的叙述中正确的是( )
在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管.下列对其作用的叙述中正确的是( )
 在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管.下列对其作用的叙述中正确的是( )
在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管.下列对其作用的叙述中正确的是( )| A. | 防止氯气造成大气污染 | |
| B. | 使反应的氯气循环使用 | |
| C. | 使烧瓶内的压强与大气压保持一致 | |
| D. | 使分液漏斗中的液体更容易注入烧瓶 |
17.在等体积、等pH的Ba(OH)2、NaOH和NH3•H2O三种溶液中,滴加等浓度的盐酸,它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
| A. | V3>V2>V1 | B. | V1>V2=V3 | C. | V3>V2=V1 | D. | V1=V2>V3 |
4.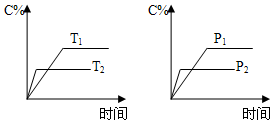 可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )
 可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g)进行过程中,当其他条件不变时,C的体积分数C%与温度(T)、压强(P)的关系如图所示.下列叙述正确的是( )| A. | 达到平衡后,加入催化剂,C的体积分数增大 | |
| B. | 达到平衡后,升高温度,平衡向左移动 | |
| C. | 化学方程式中,b>c+d | |
| D. | 达到平衡后,增加A的量,平衡向右移动 |
14.某溶液可能含有下列6种离子中的某几种:Cl-、SO42-、HCO3-、Na+、K+、Mg2+,所含离子的浓度均相等.为了确认溶液的组成,进行如下实验:
①取100mL上述溶液,加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g.
②向沉淀中加入过量的盐酸,有2.33g沉淀不溶解.
则下列结论不正确的是( )
①取100mL上述溶液,加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g.
②向沉淀中加入过量的盐酸,有2.33g沉淀不溶解.
则下列结论不正确的是( )
| A. | 原溶液一定存在SO42-、HCO3-、Mg2+,至少存在Na+、K+中的一种 | |
| B. | 若要证明原溶液中是否存在 Cl-,可在第①步的滤液中加硝酸酸化后再加硝酸银溶液 | |
| C. | 加Ba(OH)2溶液中使原溶液中的离子恰好反应且完全沉淀时,混合液呈中性 | |
| D. | 第②步实验中共消耗0.04mol HCl |
18.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,在达到平衡时,测得A的浓度降低为0.30mol/L.下列说法正确的是( )
| A. | 平衡向正反应方向移动 | B. | x+y<z | ||
| C. | B的转化率升 | D. | C的体积分数下降 |
20.有A、B、C、D、E五种常见化合物,都是由表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出C、D的化学式:CKAl(SO4)2,DCuSO4.
(2)向C溶液中加入过量E溶液,反应的离子方程式为Al3++4OH-=AlO2-+2H2O.
(3)检验C中阴离子的方法:取少量C溶液于试管中,先加稀盐酸,再加BaCl2溶液.
| 阳离子 | K+ | Na+ | Cu2+ | Al3+ |
| 阴离子 | SO42- | HCO3- | NO3- | OH- |
(1)写出C、D的化学式:CKAl(SO4)2,DCuSO4.
(2)向C溶液中加入过量E溶液,反应的离子方程式为Al3++4OH-=AlO2-+2H2O.
(3)检验C中阴离子的方法:取少量C溶液于试管中,先加稀盐酸,再加BaCl2溶液.