��Ŀ����
��Ӧ��Fe��s��+CO2��g��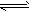 FeO��s��+CO��g�� ��H1=a kJ/mol��
FeO��s��+CO��g�� ��H1=a kJ/mol��
��CO��g��+1/2O2��g��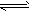 CO2��g�� ��H2=b kJ/mol
CO2��g�� ��H2=b kJ/mol
����ڲ�ͬ�¶��£���Ӧ�ٵ�ƽ�ⳣ��Kֵ���¶ȵı仯���£�

��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2 mol��L-1��CO��ƽ��Ũ��Ϊ ��
��2����Ӧ���е�a 0������ڡ���С�ڡ����ڡ�����
��3��70 0�淴Ӧ�ٴﵽƽ�⣬Ҫʹ��ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ�� ������ţ���
0�淴Ӧ�ٴﵽƽ�⣬Ҫʹ��ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ�� ������ţ���
A����С��Ӧ����� B��ͨ��CO2
C�������¶ȵ�900�� D��ʹ�ú��ʵĴ���
��4������ͼ����Ϸ�Ӧ�ٵ���__________������ţ���ͼ��v�����ʡ�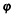 Ϊ�������CO������TΪ�¶���T1> T2��
Ϊ�������CO������TΪ�¶���T1> T2��
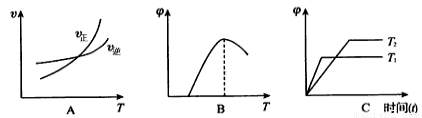
��5���ɷ�Ӧ�ٺ͢ڿ���ã�2Fe��s��+O2��g�� 2FeO��s�� ��H3���÷�Ӧ�ġ�H3= kJ/mol�����ú�a��b�Ĵ���ʽ��ʾ��
2FeO��s�� ��H3���÷�Ӧ�ġ�H3= kJ/mol�����ú�a��b�Ĵ���ʽ��ʾ��
��ϰ��ϵ�д�
�����Ŀ


 3KCl+Fe��SCN��3���ڴ���Һ�������´�����ƽ�����Ƶ��ǣ� ��
3KCl+Fe��SCN��3���ڴ���Һ�������´�����ƽ�����Ƶ��ǣ� ��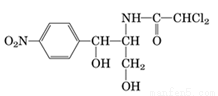
 �������й���Ҷ����������ȷ���ǣ� ��
�������й���Ҷ����������ȷ���ǣ� �� cC��g��+dD��g�� ��H��ͬʱ������ͼ�����߹��ɵ��ǣ� ��
cC��g��+dD��g�� ��H��ͬʱ������ͼ�����߹��ɵ��ǣ� ��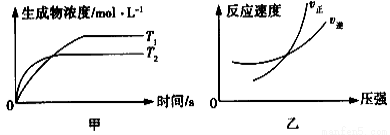
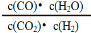 ������ʱ���¶����ߣ�H2Ũ�ȼ�С������˵����ȷ���ǣ� ��
������ʱ���¶����ߣ�H2Ũ�ȼ�С������˵����ȷ���ǣ� �� ����ѹǿ��H2Ũ��һ����С
����ѹǿ��H2Ũ��һ����С CO2��H2
CO2��H2