题目内容
下列说法中正确的是( )
| A、在原电池中,负极材料的活性一定比正极材料强 |
| B、将氯化铁溶液蒸干可得无水氯化铁固体 |
| C、反应2NO2(g)?N2O4(g)在常温下就能自发进行,则该反应的△H>0 |
| D、氯化铵溶液中加入镁,会产生两种气体 |
考点:原电池和电解池的工作原理,焓变和熵变,盐类水解的原理,盐类水解的应用
专题:
分析:A、在一些特殊电解质溶液中,负极材料的活性不一定比正极材料强;
B、氯化铁能够水解;
C、反应能否自发进行决定于焓变和熵变两方面因素;
D、氯化铵溶液水解显酸性.
B、氯化铁能够水解;
C、反应能否自发进行决定于焓变和熵变两方面因素;
D、氯化铵溶液水解显酸性.
解答:
解:A、在Al、NaOH、Mg形成的原电池中,Mg做正极.故A错误;
B、将氯化铁溶液蒸干可得无水氧化铁.故B错误;
C、2NO2(g)?N2O4(g)是放热反应,故C错误;
D、氯化铵溶液水解显酸性,加入镁会产生氢气和氨气,故D正确;
故选D.
B、将氯化铁溶液蒸干可得无水氧化铁.故B错误;
C、2NO2(g)?N2O4(g)是放热反应,故C错误;
D、氯化铵溶液水解显酸性,加入镁会产生氢气和氨气,故D正确;
故选D.
点评:本题考查了原电池有关知识,明确原电池原理是解本题关键,易错选项是A,注意原电池中负极可能被腐蚀,也可能不被腐蚀,为易错点.

练习册系列答案
相关题目
下列说法错误的是( )
| A、原子、分子、离子都可以构成物质 |
| B、由同一种元素组成的物质一定是单质 |
| C、中和反应一定是复分解反应 |
| D、置换反应中一定有单质生成 |
下列实验现象预测正确的是( )


| A、Ⅰ:振荡后静置,上层溶液颜色保持不变 |
| B、Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D、Ⅳ:继续煮沸溶液一定能得到氢氧化铁胶体 |
下列关于碳酸钠与碳酸氢钠性质的比较中,正确的是( )
| A、常温时的水溶性:Na2CO3<NaHCO3 |
| B、等物质的量时与足量酸反应产生CO2的量:Na2CO3>NaHCO3 |
| C、与等浓度稀盐酸反应的快慢:Na2CO3<NaHCO3 |
| D、同质量时消耗盐酸的量:Na2CO3<NaHCO3 |
某同学利用苹果可以制作水果原电池,如图所示.下列说法正确的是( )


| A、电流计指针偏转时,说明发生了氧化还原反应 |
| B、苹果汁中无电解质 |
| C、两个电极的材料可以相同 |
| D、水果电池工作时氧化反应和还原反应在同一处进行 |
下列说法正确的是( )
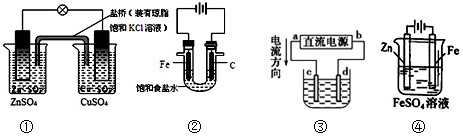

| A、图①铜锌原电池工作时,盐桥中的K+移向ZnSO4溶液 |
| B、图②装置反应一段时间,将湿润的KI淀粉试纸靠近碳电极管口,试纸变蓝 |
| C、用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
| D、用装置④可进行铁片镀锌 |
根据对角线原则,Be和Al的化学性质相似,下列说法正确是( )
| A、BeCl2溶液 pH>7,将其蒸干,灼烧后可得到BeCl2晶体 |
| B、BeCl2溶液能导电,说明BeCl2一定是离子化合物 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、Be只能与盐酸反应,不能与NaOH溶液反应 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是( )
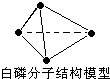

| A、31g 白磷分子(P4)中含有P-P键个数为1.5×6.02×1023 |
| B、48gO2和48gO3所含分子数为3×6.02×1023 |
| C、1.0L 1mol/L氨水中,NH3?H2O的分子数为6.02×1023 |
| D、20g 重水(D2O)中含有的中子数为8×6.02×1023 |
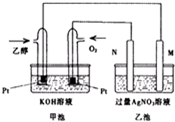 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: