题目内容
下列物质发生反应时其离子方程式正确的是( )
| A、铁与三氯化铁溶液反应:Fe+Fe3+═2Fe2+ |
| B、足量的氯气通入溴化亚铁溶液中:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| C、Fe与氢碘酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、Fe(OH)2与稀硝酸反应:Fe(OH)2+2H+═Fe2++2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电子、电荷不守恒;
B.足量氯气,亚铁离子和溴离子均全部被氧化;
C.发生氧化还原反应生成亚铁离子、氢气;
D.发生氧化还原反应生成硝酸铁、NO和水.
B.足量氯气,亚铁离子和溴离子均全部被氧化;
C.发生氧化还原反应生成亚铁离子、氢气;
D.发生氧化还原反应生成硝酸铁、NO和水.
解答:
解:A.铁与三氯化铁溶液反应的离子反应为Fe+2Fe3+═3Fe2+,故A错误;
B.足量的氯气通入溴化亚铁溶液中的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故B正确;
C.Fe与氢碘酸反应的离子反应为Fe+2H+═Fe2++H2↑,故C错误;
D.Fe(OH)2与稀硝酸反应的离子反应为3Fe(OH)2+NO3-+10H+═3Fe3++NO↑+8H2O,故D错误;
故选B.
B.足量的氯气通入溴化亚铁溶液中的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故B正确;
C.Fe与氢碘酸反应的离子反应为Fe+2H+═Fe2++H2↑,故C错误;
D.Fe(OH)2与稀硝酸反应的离子反应为3Fe(OH)2+NO3-+10H+═3Fe3++NO↑+8H2O,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
某原子可用符号
X一个该原子的基本微粒(质子、中子、电子)的总数是( )
| 19 |
| 9 |
| A、29 | B、28 | C、19 | D、9 |
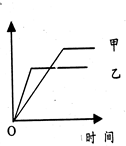 可用右侧示意图象表示的是( )
可用右侧示意图象表示的是( )| A、反应:等质量钾、钠分别与水反应,纵坐标:H 2质量,甲:钠,乙:钾 |
| B、反应:相同质量氨,在同一容器中2NH3?N2+3H2,纵坐标:氨气的转化率,甲:500℃,乙:400℃ |
| C、反应:体积比1:3的N2,H2,在体积可变的恒压容器中,2NH3?N2+3H2,纵坐标:氨气的浓度,甲:活性高的催化剂,乙:活性一般的催化剂 |
| D、反应:2mol S02与lmol 02,在相同温度下2S02+02?2S03,纵坐标:S03物质的量,甲:10atm,乙:2atm |
物质的常见分离方法有:①过滤,②蒸发,③蒸馏,④萃取,⑤分液,⑥渗析.其中根据粒子的大小进行分离的方法是( )
| A、②③ | B、⑤⑥ | C、④⑤ | D、①⑥ |
加入NaOH溶液,能使下列离子的浓度减小(不考虑溶液体积的变化)的是( )
| A、CO32- |
| B、AlO2- |
| C、SO32- |
| D、NH4+ |
2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1、CO(g)+
O2(g)=CO2(g)△H=-283kJ?mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体的H2和CO的物质的量之比( )
| 1 |
| 2 |
| A、2:1 | B、1:2 |
| C、1:1 | D、2:3 |
为了除去氯化钠中少量硫酸镁和氯化钙杂质,需进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.正确的操作顺序是( )
| A、①④②⑤③ |
| B、④①②⑤③ |
| C、②⑤④①③ |
| D、⑤②④①③ |