题目内容
在同温同压下,合成氨反应N2+3H2=2NH3进行到某时刻达到平衡.起始时N2和H2共120体积,平衡时总体积为70体积,则原混合气体中N2和H2的体积比可能为:
A.1:3 B.9:15 C.5:19 D.1:1
A
【解析】
试题分析:根据差量法来计算,起始是共120体积,平衡时为70体积,体积减少了50体积
N2 + 3H2 = 2NH3 △ V(减少)
1 3 2 2
25 75 50 50,所以反应后总体积要减少50体积的话,N2要消耗25体积, H2 要消耗75体积,A项N2和H2的体积比为1:3,那么N2和H2的体积分别是30体积、90体积,可以满足反应的消耗量,对;B项N2和H2的体积比为9:15,那么N2和H2的体积分别是45体积、75体积,那么H2就反应完了,反应是可逆反应,不可能完全反应,错;C项N2和H2的的体积比为5:19,N2和H2的体积分别是25体积、95体积,N2的量不够消耗,错;D项、N2和H2的体积比为1︰1,N2和H2的体积分别是60体积、60体积,H2的量不够消耗,错。
考点:差量法的使用和可逆反应的特点。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 N2O4(g)
N2O4(g) 

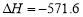 kJ·mol-1
kJ·mol-1 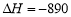 kJ·mol-1
kJ·mol-1