题目内容
向2L密闭容器中通入amol 气体 A和bmol气体B,在一定条件下发生反应:
xA(g)+ yB(g) pC(g) + qD(g)。已知:平均反应速率V(C) =1/2V(A) ;反应2min 时,A的浓度减少了1/3 ,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:
pC(g) + qD(g)。已知:平均反应速率V(C) =1/2V(A) ;反应2min 时,A的浓度减少了1/3 ,B的物质的量减少了a/2 mol,有a mol D生成。回答下列问题:
(1)反应2min内,A的平均反应速率是 mol?L-1?min-1;
(2)原化学方程式中,化学计量数是:
A(g)+ B(g)  C(g) + D(g)
C(g) + D(g)
(3)反应平衡时,D为2a mol,则B的转化率为 ;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应
的△H 0;(填“>”、“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
①反应速率增大 ,理由是体积减小,反应物的浓度增大,因而使反应速率增大;
②平衡时反应物的转化率 (填“增大”、“减小”或“不变”),理由是
(1)a/12 (2)2 3 1 6 (3)a/b (4)<
(5)减小 缩小体积相当增大压强,平衡向气体分子数减小的方向移动
【解析】
试题分析:(1)A的浓度减少了1/3 ,则用A表示的反应速率是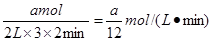 。
。
(2)A的物质的量减少了a/3 mol,B的物质的量减少了a/2 mol,有a mol D生成,所以根据物质的量的变化量之比等于相应的化学计量数之比可知,x:y:q=2:3:6。又因为V(C) =1/2V(A) ,所以2p=x,因此该反应的化学方程式是2A(g)+3B(g)  C(g) + 6D(g).
C(g) + 6D(g).
(3)反应平衡时,D为2a mol,则根据方程式可知,消耗B是amol,则B的转化率为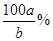 。
。
(4)只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,这说明升高温度,平衡显逆反应方向移动,所以正反应是放热反应,则△H<0.
(5)缩小体积相当增大压强,平衡向气体分子数减小的方向移动,即向逆反应方向移动,所以转化率降低。
考点:考查可逆反应的有关判断、计算,外界条件对平衡状态的影响和反应热的判断
点评:该题是中等难度的试题,试题综合性强,贴近高考。试题注重基础知识的检验,侧重考查学生灵活运用基础知识解决实际问题的能力。有利于培养学生的逻辑推理能力和发散思维能力,提高学生的应试能力和学习效率。

 阅读快车系列答案
阅读快车系列答案

 2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。
2NH3(g);已知:反应2min达到平衡 ,此时N2的浓度减少了2/3。