题目内容
17.依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是( )| A. | 卤素单质 Cl2、Br2、I2的氧化性强弱 | |
| B. | 气态氢化物 NH3、H2O、HF 的稳定性 | |
| C. | 碱金属单质 Li、Na、K 与水反应的剧烈程度 | |
| D. | 1mol Na、Mg、Al 分别与足量盐酸反应时失电子数的多少 |
分析 A.卤素单质的氧化性越强,对应元素的非金属性越强;
B.简单氢化物的稳定性越强,非金属性越强;
C.金属单质与水反应越剧烈,对应元素的金属性越强;
D.金属性强弱与得失电子的多少没有必然关系.
解答 解:A.卤素元素中,单质氧化性越弱,对应元素的非金属性越强,可根据 Cl2、Br2、I2的氧化性强弱判断卤素的非金属性强弱,故A正确;
B.气态氢化物NH3、H2O、HF的稳定性越强,非金属性越强,可根据气态氢化物稳定性判断元素非金属性,故B正确;
C.金属单质与水反应越剧烈,对应元素金属性越强,可根据碱金属单质 Li、Na、K 与水反应的剧烈程度判断元素金属性强弱,故C正确;
D.金属性强弱与失去电子的能力有关,与得失电子数目无关,不能根据1mol Na、Mg、Al 分别与足量盐酸反应时失电子数的多少判断金属性强弱,故D错误;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度不大,明确元素周期律内容为解答关键,注意掌握判断元素金属性、非金属性强弱的方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
7.在一定温度下,将气体X和气体Y 各0.16mol充入10L 恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,反应过程中测定的数据如表( )
下列判断正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,平衡向正反应方向移动 | |
| C. | 当进行4分钟时,反应已达平衡状态 | |
| D. | 其他条件不变,通过缩小容器体积增大压强,平衡常数减小 |
8.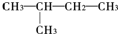 的一氯取代物的种数是( )
的一氯取代物的种数是( )
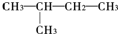 的一氯取代物的种数是( )
的一氯取代物的种数是( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
12.两片铁片分别与足量的盐酸和氯气完全反应,生成的氢气和消耗的氯气体积相同(在相同条件下),则两片铁片的质量比为( )
| A. | 1:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
2.对于某些离子的检验方法(包括操作、现象、结论),完全正确的是( )
| A. | 向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,一定有 Al3+ | |
| C. | 向待测溶液中先滴加盐酸酸化未出现沉淀,再加入 BaCl2 溶液有白色沉淀产生,一定有SO42- | |
| D. | 向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+ |
9.下列有机化合物中,既能与盐酸起反应,又能与NaOH溶液反应的是( )
| A. | 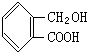 | B. | 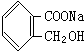 | C. | H2NCH2COONa | D. | H2NCH2COOH |
6.在碱性条件下,1mol某饱和羧酸酯完全水解可得到1mol甘油和3mol羧酸钠,且羧酸钠酸化后的产物与戊醇的相对分子质量相等,则该饱和羧酸酯的分子式为( )
| A. | C12H20O6 | B. | C15H26O6 | C. | C18H32O6 | D. | C21H38O6 |