题目内容
20.配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合.如NH${\;}_{4}^{+}$就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的.据此,回答下列问题:(1)下列粒子中可能存在配位键的是BD
A.CO2 B.H3O+ C.CH4 D.[Ag(NH3)2]+
(2)向硫酸铜溶液中滴加氨水,会有蓝色沉淀产生,继续滴加,沉淀溶解,溶液变成深蓝色.请写出其中发生反应的离子方程式Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- 或Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
(3)请写出铜原子的核外电子排布式1s22s22p63s23p63d104s1.
(4)配位化学创始人维尔纳发现,将各为1mol的CoCl3•6NH3(黄色)、CoCl3•5NH3(紫红色)、CoCl3•4NH3(绿色)、CoCl3•4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol.已知上述配合物中配离子的配位数均为6.请根据实验事实用配合物的形式写出它们的化学式.
①CoCl3•5NH3[Co(NH3)5Cl]Cl2、②CoCl3•4NH3(紫色)[Co(NH3)4Cl2]Cl.
分析 (1)含有孤电子对和含有空轨道的原子之间易形成配位键;
(2)硫酸铜和氨水反应生成铵根离子和氢氧化铜沉淀,氢氧化铜和氨水继续反应生成铜氨络合物;
(3)铜是29号元素,核外有29个电子,根据核外电子排布式规则书写;
(4)1mol的CoCl3•6NH3(黄色)、CoCl3•5NH3(紫红色)、CoCl3•4NH3(绿色)、CoCl3•4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol,说明这几种配合物的外界中氯离子个数分别是3、2、1、1,剩余氯离子为配体,再结合配合物的配位数确定化学式.
解答 解:(1)含有孤电子对和含有空轨道的原子之间易形成配位键,
A.CO2中没有孤电子对和空轨道,所以没有配位键,故错误;
B.H3O+中一个H原子含有空轨道、O原子含有孤电子对,所以该微粒中含有配位键,故正确;
C.CH4中没有孤电子对和空轨道,所以没有配位键,故错误;
D.[Ag(NH3)2]+中银离子含有空轨道、N原子含有孤电子对,所以该微粒中含有配位键,故正确;
故答案为:BD;
(2)硫酸铜和氨水反应生成铵根离子和氢氧化铜沉淀,离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;继续滴加,氢氧化铜和氨水继续反应生成铜氨络合物,离子方程式为Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- 或Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O,沉淀溶解,溶液变成深蓝色,
故答案为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- 或Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O;
(3)铜是29号元素,核外有29个电子,满足全满半满的稳定结构,其核外电子排布式是1s22s22p63s23p63d104s1,轨道式为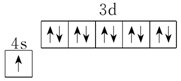 ,
,
故答案为:1s22s22p63s23p63d104s1;
(4)1mol的CoCl3•6NH3(黄色)、CoCl3•5NH3(紫红色)、CoCl3•4NH3(绿色)、CoCl3•4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol,说明这几种配合物的外界中氯离子个数分别是3、2、1、1,剩余氯离子为配体,
①CoCl3•5NH3的外界中含有2个氯离子,则另外一个氯原子为配体,该化合物的配合物是6,则氨气分子都是配体,则其化学式为[Co(NH3)5Cl]Cl2,
故答案为:[Co(NH3)5Cl]Cl2;
②CoCl3•4NH3中氯离子个数是1,则另外两个氯原子为配体,其配位数是6,则氨气分子都是配体,则该化学式为[Co(NH3)4Cl2]Cl,
故答案为:[Co(NH3)4Cl2]Cl.
点评 本题考查了配合物,明确配位键的形成条件、配合物的內界及外界的性质是解本题关键,只有外界能发生电离生成离子,內界不发生电离,为易错点,题目难度中等.

| A. | 等浓度的 CH3COOH 与 KOH 任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) | |
| B. | 在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7 | |
| C. | 浓度均为 0.1 mol/L 的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者 | |
| D. | 常温下 pH 为 5 的盐酸溶液稀释 1000 倍后,pH 等于 8 |
| A. | Na、K--遇湿易燃物品 | B. | TNT、NH4NO3--爆炸品 | ||
| C. | CH4、C2H5OH--易燃气体 | D. | 浓H2SO4、浓HNO3--腐蚀品 |
| A. | 用酸性KMnO4溶液鉴别乙烯和乙醇 | |
| B. | 将乙烷与溴水混合光照制溴乙烷 | |
| C. | 苯和硝基苯的混合物采用分液的方法分离 | |
| D. | 可用CCl4萃取碘水中的碘 |
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
| A. | NaBr: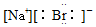 | B. | MgCl2: | C. | KCl: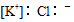 | D. | Na2O2: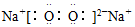 |
| A. | 随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 | |
| B. | 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 | |
| C. | 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)重复出现 | |
| D. | 随着元素原子序数的递增,元素的金属性逐渐减弱,非金属性逐渐增强重复出现 |

| A. | 该混合物一定是K2CO3和NaCl | B. | 该混合物可能是Na2CO3和KCl | ||
| C. | 该混合物可能是Na2SO4和Na2CO3 | D. | 该混合物一定是Na2CO3和NaCl |
| A. | 乙醇的结构简式为CH3CH2OH,分子式为C2H5OH | |
| B. | 乙酸的电离方程式为CH3COOH=CH3COO-+H+ | |
| C. | 中子数为16的磷原子可表示为${\;}_{15}^{31}$P | |
| D. | S2-结构示意图为 |