题目内容
12.把23g钠投入到m1 g足量的水中得到a g溶液,把24g镁投入到m2 g足量的盐酸中得到b g溶液,若m1=m2,则a,b的关系是( )| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
分析 发生反应:2Na+2H2O=2NaOH+H2↑、Mg+2HCl=MgCl2+H2↑,表示出各自反应生成氢气的质量,溶液质量=金属质量+水的质量-生成氢气的质量.
解答 解:由2Na+2H2O=2NaOH+H2↑,可知23g钠反应生成氢气为:$\frac{23g×2}{46}$=1g,故a=23+m1-1=(m1+22),
由Mg+2HCl=MgCl2+H2↑,可知24gMg反应生成为:$\frac{24g×2}{24}$=2g,故b=24+m2-2=(m2+22),
若m1=m2,则a=b,
故选C.
点评 本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,关键明确溶液质量计算,可以利用差量法进行分析解答,难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
4.化学在生产和生活中有着重要的作用,下列有关说法不正确的是( )
| A. | 小苏打可用作糕点的膨化剂 | |
| B. | “地沟油“经过加工处理可用来制肥皂 | |
| C. | 多地花重金购买“雾霾消除车“,从根本上缓解了雾霾问题 | |
| D. | 装饰材料释放的苯、甲苯、甲醛等易挥发性物质会导致室内空气污染 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 60g丙醇含有的共价键数目为10NA | |
| B. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子数为0.3NA | |
| C. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| D. | 80ml10mol/L盐酸与足量MnO2加热反应,产生Cl2的分子数为0.2NA |
17.在两个密闭容器中,分别充满等物质的量的甲、乙两种气体,它们的温度和摩尔质量均相同.试根据甲、乙的密度(ρ)的关系,下列说法中正确的是( )
| A. | 若ρ(甲)<ρ(乙),则气体的压强:甲>乙 | B. | 若ρ(甲)>ρ(乙),则分子数:甲>乙 | ||
| C. | 若ρ(甲)<ρ(乙),则气体摩尔体积:甲<乙 | D. | 若ρ(甲)>ρ(乙),则气体体积:甲<乙 |
 .
.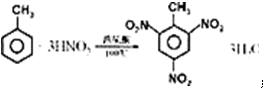 .
.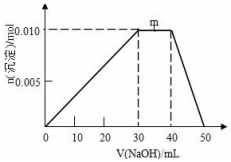 向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下: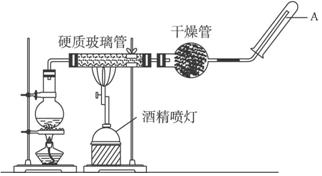 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.