题目内容
18.目前从海水提溴(Br2)大致有以下步骤.(1)向浓缩的海水中通入某种气体,将海水中的Br-氧化为Br2,该气体是Cl2.
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3.1moL Br2需消耗Na2CO31moL.
(3)再将所得混合溶液用稀硫酸酸化,得到浓度较高的溴水,配平该反应的离子方程式.
5Br-+1 BrO3-+6H+→3 Br2+3H2O.
分析 (1)氯气具有氧化性,能氧化溴离子生成单质溴;
(2)用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,结合质量守恒书写反应的离子方程式,结合定量关系计算;
(3)Br-、BrO3-在酸性条件下发生反应生成Br2,溴元素化合价-1价和+5价变化为0价,电子转移总数5,结合电子守恒和原子守恒配平.
解答 解:(1)向浓缩的海水中通入某种气体,将海水中的Br-氧化为Br2,该气体是氯气,
故答案为:Cl2;
(2)用热空气将Br2从上述溶液中吹出,并由浓Na2CO3溶液吸收,溴歧化为Br-和BrO3-,反应的离子方程式为3Br2+3CO32-═5Br-+BrO3-+3CO2 ,1moL Br2需消耗Na2CO3物质的量为1mol,
故答案为:1;
(3)Br-、BrO3-在酸性条件下发生反应生成Br2,溴元素化合价-1价和+5价变化为0价,电子转移总数5,得到离子方程式为:Br-+BrO3-+6H+=3Br2+3H2O
故答案为:5、1、6、3、3.
点评 本题考查海水资源的综合利用,为高频考点,侧重于学生的分析能力和实验能力的考查、氧化还原反应电子转移数,注意把握相关物质的性质,为解答该题的关键,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
16.一种铂(Pt)原子的质量数是196,质子数比中子数少40.该原子的核素符号是( )
| A. | ${\;}_{118}^{78}$Pt | B. | ${\;}_{78}^{118}$Pt | C. | ${\;}_{78}^{196}$Pt | D. | ${\;}_{118}^{196}$Pt |
6.酸雨形成的主要原因是( )
| A. | 火山爆发产生的气体 | B. | 大气中二氧化碳含量增加 | ||
| C. | 乱砍乱伐森林,破坏了生态环境 | D. | 工业上大量燃烧含硫燃料 |
13.在生产和生活上应用的含氯消毒剂、漂白剂有多种,如HClO、NaClO、ClO2等.
(1)氯气是合成含氯消毒剂的原料.在催化剂、420℃的条件下,氧气与氯化氢气体反应可置换出氯气,利用表数据写出该反应的热化学方程式O2(g)+4HCl(g)=2Cl2(g)+2H2O(g)△H=-133KJ/mol.
(2)氯气溶于水,发生Cl2+H2O═H++Cl-+HC1O,则该反应的平衡常数表达式K=$\frac{c({H}^{+})c(C{l}^{-})c(HClO)}{c(C{l}_{2})}$.下列关于氯水的叙述正确的是AD(填写序号).
A.向氯水中加入少量Na2CO3粉末,其漂白性增强
B.向氯水中通人氯气,c(H+)/c(ClO-)减小
C.加水稀释氯水,溶液中的所有离子浓度均减小
D.加水稀释氯水,水的电离平衡向正反应方向移动
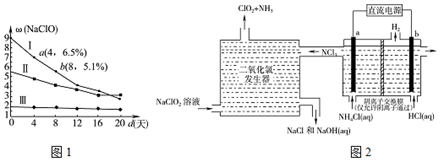
(3)漂白液的有效成分是NaClO,研究漂白液的稳定性对
其生产和保存有实际意义.图1是30℃时,三种漂白液中NaClO的质量分数随时间的变化关系.
①分解速率v(I)>v(Ⅱ)(填“>”“<”或“=”)
②漂白液I在4~8天内的分解速率为3.5g'L-l.d-1.(常温下漂白液的密度近似等于1g•cm-3,溶液体积变化忽略不计)
(4)ClO2是一种安全稳定的消毒剂.工业上通过惰性电极电解氯化铵和盐酸的方法制备ClO2,原理如图2:
①a电极上产生的NCl3分子,常温下是一种黄色粘稠的油状液体,该分子的电子式为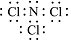 .
.
②电解池中总反应的离子方程式为NH4++2H++3Cl-$\frac{\underline{\;通电\;}}{\;}$NCl3+3H2↑.
③若电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则理论上b电极上产生氢气的质量为
0.6g.
(1)氯气是合成含氯消毒剂的原料.在催化剂、420℃的条件下,氧气与氯化氢气体反应可置换出氯气,利用表数据写出该反应的热化学方程式O2(g)+4HCl(g)=2Cl2(g)+2H2O(g)△H=-133KJ/mol.
| 化学键 | Cl-Cl | O=O | O-H | H-Cl |
| 键能(kJ.mol-1) | 247 | 498 | 463 | 431 |

A.向氯水中加入少量Na2CO3粉末,其漂白性增强
B.向氯水中通人氯气,c(H+)/c(ClO-)减小
C.加水稀释氯水,溶液中的所有离子浓度均减小
D.加水稀释氯水,水的电离平衡向正反应方向移动
(3)漂白液的有效成分是NaClO,研究漂白液的稳定性对
其生产和保存有实际意义.图1是30℃时,三种漂白液中NaClO的质量分数随时间的变化关系.
①分解速率v(I)>v(Ⅱ)(填“>”“<”或“=”)
②漂白液I在4~8天内的分解速率为3.5g'L-l.d-1.(常温下漂白液的密度近似等于1g•cm-3,溶液体积变化忽略不计)
(4)ClO2是一种安全稳定的消毒剂.工业上通过惰性电极电解氯化铵和盐酸的方法制备ClO2,原理如图2:
①a电极上产生的NCl3分子,常温下是一种黄色粘稠的油状液体,该分子的电子式为
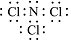 .
.②电解池中总反应的离子方程式为NH4++2H++3Cl-$\frac{\underline{\;通电\;}}{\;}$NCl3+3H2↑.
③若电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则理论上b电极上产生氢气的质量为
0.6g.
3.下列实验“操作和现象”与“结论”对应关系正确的是( )
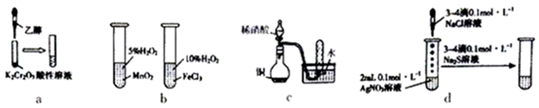

| A. | a图,滴加乙醇,试管中橙色溶液变为绿色,乙醇发生取代反应生成乙酸 | |
| B. | b图,左边试管中产生气泡迅速,说明二氧化锰的催化效果比氯化铁好 | |
| C. | c图,根据试管中收集到无色气体,能验证铜与稀硝酸的反应产物是NO | |
| D. | d图,试管中先有白色沉淀,后有黑色沉淀生成,能确定Ksp(AgCl)>Ksp(Ag2S) |
10.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 CaCl2溶液等体积混合:c(Na+)+c(Ca2+)═c(CH3COO-)+c(CH3COOH)+c(Cl-) | |
| B. | 少量Cl2通入过量泠的0.1 mol•L-1 NaOH溶液中:c(Na+)═c(HClO)+c(ClO-)+c(Cl-) | |
| C. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1 HCl溶液混合至pH=7:c(Na+)>c(Cl-)═c(CH3COOH) | |
| D. | 0.2 mol•L-1 NH3•H2O溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Cl-)+c(H+)═c(NH3•H2O)+c(OH-) |
7.设NA为阿移伽德罗常数的值,下列说法正确的是( )
| A. | 1LpH=1的硫酸溶液中含有的H+数为0.2NA | |
| B. | 12g石墨和C60的混合物中质子总数为6NA | |
| C. | lmolNa2O2和足量的水完全反应,转移电子数为2NA | |
| D. | 2mol热的浓硫酸与足量Cu充分反应生成的SO2在标准状况下的体积约为22.4L |