题目内容
2.下列物质中,有非极性键的是( )| A. | 氮气 | B. | 氯化镁 | C. | 水 | D. | 甲烷 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,同种非金属形成非极性共价键,以此来解答.
解答 解:A.只含氮氮非极性共价键,故A选;
B.只含镁离子与氯离子之间的离子键,故B不选;
C.含离子键和O-H极性键,故C不选;
D.只含H-C极性共价键,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
相关题目
12.下列离子反应方程式正确的是( )
| A. | 少量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| B. | 碳酸钙与稀盐酸混合:CO32-+2H+═CO2↑+H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Al2O3溶于NaOH溶液中:Al2O3+2OH-═2[Al(OH)4]- |
13.在恒温恒容密闭容器中发生反应NH2COONH4(s)?2NH3(g)+CO2(g),不能判断该反应已达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | |
| B. | 密闭容器中总压强不变 | |
| C. | 密闭容器中混合气体的密度不变 | |
| D. | 密闭容器中混合气体的平均摩尔质量不变 |
14.下列说法正确的是( )
| A. | 0.1 mol•L-1的醋酸加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
7.下列说法正确的是( )
| A. | 干冰升华时须吸收大量的热,这就是化学反应中的吸热现象 | |
| B. | 酒精常被用作酒精灯和内燃机的燃料,说明酒精燃烧是放热反应 | |
| C. | 木炭常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应 | |
| D. | 酸碱中和反应都放热,因此可以将其设计成原电池,将化学能转换成电能供人们使用 |
 .
.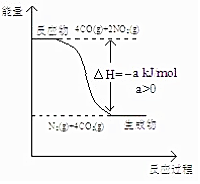 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.
研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.