题目内容
20.下列不是海水淡化方法的是( )| A. | 蒸馏法 | B. | 电渗析法 | C. | 离子交换法 | D. | 萃取法 |
分析 海水淡化海水就是将海水中的可溶性杂质除去的过程,可根据淡化原理进行分析解答.
解答 解:A.蒸馏法是把水从水的混合物中分离出来,得到纯净的水,故A正确;
B.利用电渗析法可使相应的离子通过半透膜以达到硬水软化的效果,故B正确;
C.通过离子交换树脂可以除去海水中的离子,从而达到淡化海水的目的,故C正确;
D.对于微溶于水的有机物,可用萃取法,水中没有微溶于水的有机物,故D错误;
故选D.
点评 本题考查了海水的淡化方法,题目难度不大,注意掌握海水淡化方法常用方法,如海水冻结法、电渗析法、蒸馏法、反渗透法等,其中最常用的有蒸馏法、反渗透法.

练习册系列答案
相关题目
8.下面有四种有机物,用提供的试剂分别鉴别,将所用试剂及产生的现象的序号填在相应横线上.
①cB②bC③dA④aD
①cB②bC③dA④aD
| 有机物 | 试剂 | 现象 |
| ①淀粉 ②苯乙烯 ③苯酚 ④蛋白质 | a.浓硝酸 b.酸性高锰酸钾溶液 c.碘水 d.FeCl3溶液 | A.呈紫色 B.呈蓝色 C.紫色褪去 D.呈黄色 |
5.我国正在推广使用乙醇汽油;所谓乙醇汽油就是在汽油中加入适量乙醇(一般为10:1)混合而成的一种燃料.下列有关的叙述错误的是( )
| A. | 由石油可以制得汽油 | |
| B. | 乙醇汽油是一种新型的化合物 | |
| C. | 汽车使用乙醇汽油可以减少有害气体的排放 | |
| D. | 由玉米、高梁发酵可以制得乙醇 |
12.聚异丁烯( )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
 )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )| A. | 聚异丁烯可以通过加聚反应制得 | |
| B. | 聚异丁烯的分子式为(C4H8)n | |
| C. | 聚异丁烯能使溴的四氯化碳溶液褪色 | |
| D. | 聚异丁烯完全燃烧生成CO2 和H2O的物质的量相等 |
9.工业上常用如下的方法从海水中提溴:浓缩海水$→_{①}^{氯气}$ 粗产品溴$→_{②}^{通空气和水蒸气}$溴蒸气$→_{③}^{SO_{2}}$物质X$→_{④}^{氯气}$产品溴,下列说法错误的是( )
| A. | 步骤①的主要反应为:Cl2+2Br-→Br2+2Cl- | |
| B. | 物质X为HBrO | |
| C. | 步骤②③的目的是富集溴元素 | |
| D. | 步骤②利用了溴易挥发的性质 |
10.下列措施不合理的是( )
| A. | 用SO2漂白纸浆、毛、丝等 | B. | 用焦炭高温还原SiO2制粗硅 | ||
| C. | 用明矾对自来水进行杀菌消毒 | D. | 用Na2S作沉淀剂除去污水中的Hg2+ |
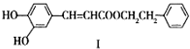 不饱和酯类化合物在药物、涂料等方面应用广泛.
不饱和酯类化合物在药物、涂料等方面应用广泛. .
.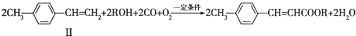
 (写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.
(写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.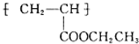 可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.
可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.