题目内容
X、Y、Z是3种短周期元素,其中X、Y位于同一周期,Y、Z处于同一主族.X原子的最外层电子数是其核外电子总数的
倍.Z原子的最外层电子数比X少1.下列说法中不正确的是( )
| 3 |
| 4 |
| A、元素的非金属性由弱到强的顺序为:Z<Y<X |
| B、3种元素的最简单氢化物的沸点由高到低的顺序为:X>Z>Y |
| C、3种元素的原子半径由大到小的顺序为:Z>Y>X |
| D、Y元素的最高价氧化物的水化物与其最低价氢化物可以化合成盐 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z是3种短周期元素,X原子的最外层电子数是其核外电子总数的
倍,最外层电子不超过8个、K层为最外层不超过2个,所以X是O元素;Z原子的最外层电子数比X少1,则Z最外层电子数为5,Y、Z处于同一主族,则Y最外层电子数为4,X和Y位于同一周期,所以Y为N元素,则Z为P元素,
A.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱;
B.结构相似的氢化物熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高;
C.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
D.铵盐可以有N元素的氢化物和其最高价氧化物的水化物化合而成.
| 3 |
| 4 |
A.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱;
B.结构相似的氢化物熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高;
C.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
D.铵盐可以有N元素的氢化物和其最高价氧化物的水化物化合而成.
解答:
解:X、Y、Z是3种短周期元素,X原子的最外层电子数是其核外电子总数的
倍,最外层电子不超过8个、K层为最外层不超过2个,所以X是O元素;Z原子的最外层电子数比X少1,则Z最外层电子数为5,Y、Z处于同一主族,则Y最外层电子数为4,X和Y位于同一周期,所以Y为N元素,则Z为P元素,
A.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,所以非金属性Z<Y<X,故A正确;
B.结构相似的氢化物熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高,氨气中存在氢键,磷化氢中不存在氢键,所以氢化物的熔沸点Y>Z,故B错误;
C.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径Z>Y>X,故C正确;
D.N元素的最高价氧化物的水化物是硝酸、最低价氢化物是氨气,二者发生化合反应生成硝酸铵,故D正确;
故选B.
| 3 |
| 4 |
A.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,所以非金属性Z<Y<X,故A正确;
B.结构相似的氢化物熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高,氨气中存在氢键,磷化氢中不存在氢键,所以氢化物的熔沸点Y>Z,故B错误;
C.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径Z>Y>X,故C正确;
D.N元素的最高价氧化物的水化物是硝酸、最低价氢化物是氨气,二者发生化合反应生成硝酸铵,故D正确;
故选B.
点评:本题考查原子结构和元素周期律,侧重考查原子结构、元素周期律、氢键等知识点,明确同一主族、同一周期原子结构、元素周期律即可解答,注意氢键对物质熔沸点的影响,题目难度不大.

练习册系列答案
相关题目
 向500mL某碳酸钠溶液中逐滴加入1mol/L的盐酸,测得溶液中溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是 ( )
向500mL某碳酸钠溶液中逐滴加入1mol/L的盐酸,测得溶液中溶液中Cl─、HCO3─的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是 ( )| A、Oa段与ab段反应的离子方程式均为:CO32-+H+=HCO3- |
| B、该碳酸钠溶液的物质的量浓度为0.5mol/L |
| C、b点时,滴加盐酸的体积为600mL |
| D、b点时生成CO2的物质的量为0.3 mol |
汽车尾气净化中的一个反应如下:NO(g)+CO(g)?
N2(g)+CO2 (g)△H=-373.4kJ.mol-1若反应在恒容的密闭容器中达到平衡状态,下列有关说法正确的是( )
| 1 |
| 2 |
| A、其它条件不变,加入催化剂,△H变大 |
| B、及时除去二氧化碳,正反应速率加快 |
| C、降低温度,可提高反应物的转化率 |
| D、若气体的密度保持不变,说明平衡不发生移动 |
下列离子方程式正确的是( )
| A、向次氯酸钙溶液通入少量CO2:2ClO-+H2O+CO2=CO32-+2HClO |
| B、向明矾溶液中加入足量Ba(OH)2溶液:Al3++2SO42-+4OH-+2Ba2+=2BaSO4↓+[Al(OH)4]- |
| C、向FeCl3溶液中加入足量单质锌:Zn+2Fe3+=Zn2++2Fe2+ |
| D、向NaHSO4中滴加Ba(OH)2溶液至中性:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
 是一种局部麻醉药物,可由下列路线合成:
是一种局部麻醉药物,可由下列路线合成:
 的合成路线流程图(元机试剂任选).合成路线流程图示例如下:C2H5OH
的合成路线流程图(元机试剂任选).合成路线流程图示例如下:C2H5OH
 合成
合成 (部分试剂和反应条件已去).请回答下列问题:
(部分试剂和反应条件已去).请回答下列问题: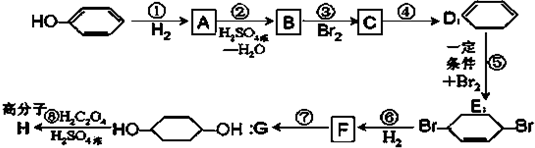
 ,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:
,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式: 的化学方程式(有机物写结构简式,注明反应条件).
的化学方程式(有机物写结构简式,注明反应条件). ,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是
,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是 B.
B. C.
C. D.
D.